ESTIMACIÓN DE LA INCERTIDUMBRE DE LA MEDICIÓN EN LA DETERMINACIÓN DE GLUCOSA EN SANGRE POR EL MÉTODO FOTOMÉTRICO ENZIMÁTICO GOD–PAP
ESTIMATION OF THE UNCERTAINTY OF MEASUREMENT IN THE DETERMINATION OF GLUCOSE IN BLOOD BY THE ENZYMATIC PHOTOMETRIC METHOD GOD – PAP
Víctor Manuel Castro Malabrigo 1 *, Patricia Elizabeth Torres Plasencia 1, Alvaro David Rodríguez Salvatierra 2, Orlando Enrique Pretel Sevillano 1, Luis Miguel Castañeda Pelaez 3
1 Departamento de Química Biológica y Fisiología Animal, Facultad de Ciencias Biológicas, Universidad Nacional de Trujillo, Av. Juan Pablo II s/n – Ciudad Universitaria, Trujillo, Perú.
2 Escuela de Posgrado de la Universidad Nacional de Trujillo.
3 Facultad de Ciencias de la Salud, Universidad Privada del Norte, Lima- Perú.
Artículo original:
Recibido: 16 de setiembre 2020
Aceptado: 17 de mayo 2021
Resumen
Este trabajo tuvo como objetivo, estimar la incertidumbre de la medición en la determinación de glucosa en sangre por el método fotométrico enzimático GOD-PAP; esta investigación, resulta de gran utilidad para los laboratorios de análisis clínicos, porque garantiza la calidad, exactitud y confiabilidad de los resultados para el diagnóstico de la diabetes. Se utilizaron tres muestras de sangre, obtenidas en tres días consecutivos, las que se analizaron por triplicado; el cálculo de la incertidumbre, se basó en la metodología descrita en “Quantifying Uncertainty in Analytical Measurement-Guía CG 4 EURACHEM/CITAC”. El valor de la incertidumbre expandida, calculada por la ley de propagación de la incertidumbre fue 2,3 mg/dL para un factor de cobertura (k) de 2 al 95% de nivel de confianza y, la concentración de glucosa en sangre fue de 95,9 mg/dL. Se evaluaron las fuentes de incertidumbre y se demostró que solamente la pureza del reactivo y la temperatura a la cual se realizó las mediciones influyen significativamente en la incertidumbre de los resultados.
Palabras clave: glucosa, incertidumbre expandida, método fotométrico enzimático GOD-PAP
Abstract
The objective of this work was to estimate the uncertainty of the measurement in the determination of glucose in blood by the enzymatic photometric method GOD-PAP; this research is very useful for clinical analysis laboratories, because it guarantees the quality, accuracy and reliability of the results for the diagnosis of diabetes. Three blood samples were used, obtained on three consecutive days, which were analyzed in triplicate; the uncertainty calculation was based on the methodology described in “Quantifying Uncertainty in Analytical Measurement - Guide CG 4 EURACHEM/CITAC”. The value of the expanded uncertainty, calculated by the law of propagation of uncertainty, was 2.3 mg/dL for a coverage factor (k) of 2 at 95% confidence level, and the blood glucose concentration was 95.9 mg/dL. The sources of uncertainty were evaluated and it was shown that only the purity of the reagent and the temperature at which the measurements were made, significantly influence the uncertainty of the results.
Keywords: Expanded uncertainty, enzymatic photometric method GOD-PAP, glucose
* Autor correspondiente: E mail: vcastrom@unitru.edu.pe
DOI: http://dx.doi.org/10.17268/rebiol.2021.41.01.08
Citar como:
Castro, V., Torres P., Rodríguez, A., Pretel, O., & Castañeda, L. 2021. Estimación de la incertidumbre de la medición en la determinación de glucosa en sangre por el método fotométrico enzimático GOD–PAP. REBIOL, 41(1):75-90.
1. Introducción
El análisis de glucosa en sangre se utiliza para detectar tanto la hiperglucemia como la hipoglucemia lo cual tiene relevancia para el diagnóstico y manejo de la diabetes. Los análisis enzimáticos de glucosa se basan en los dos métodos más comúnmente empleados en química clínica, el "método de la hexoquinasa" y el "método de la glucosa oxidasa GOD-PAP" (Duxbury, 2006). Estevinho et al. (2013) demostró que el método enzimático es más adecuado que la cromatografía líquida de alto rendimiento (HPLC), porque permite analizar una gran cantidad de muestras y el resultado es más rápido.
Para el diagnóstico de enfermedades, el médico clínico, solicita pruebas a los laboratorios clínicos (Ventura et al., 2007). La función del laboratorio clínico es analizar muestras de pacientes con el fin de obtener información; dicha información contribuye a diagnosticar, seguir la evolución, controlar tratamientos y/o prevenir enfermedades (San Román, 2009), la presencia de cualquier tipo de error en el proceso de medición en el laboratorio clínico se refleja en el resultado final; la emisión de resultados poco confiables, puede conducir a equivocaciones que afectan negativamente al proceso diagnóstico, con el consiguiente riesgo potencial para los pacientes (Ventura et al., 2007).
Actualmente hay una necesidad por parte de los laboratorios clínicos de implementar medidas que permitan asegurar la capacidad de proporcionar datos con la calidad requerida por sus clientes a través de la trazabilidad de las mediciones. Por lo tanto, es necesario que exista un procedimiento fácil de usar y aceptado de manera general para caracterizar la calidad del resultado de una medición, esto es, para estimar y expresar su incertidumbre (Milinkovi et al., 2018), que, por definición, es un parámetro asociado al resultado de una medición que caracteriza la dispersión de los valores que podrían razonablemente atribuirse al mensurando (VIM, 2012; Milinkovi et al., 2018; Martinello et al., 2019).
La estimación de la incertidumbre, se realiza a través de dos enfoques: intralaboratorio, utilizando datos propios del laboratorio e, interlaboratorio, utilizando datos propios del laboratorio y datos colaborativos con otras instituciones. A nivel intralaboratorio, la incertidumbre se determina generalmente, utilizando el enfoque de modelamiento, que involucra 4 pasos: (i) especificar el mensurado, (ii) identificar las fuentes de incertidumbre, (iii) cuantificar los componentes de la incertidumbre, (iv) calcular la incertidumbre combinada y la incertidumbre expandida (EURACHEM/CITAC CG4 et al., 2012). La estimación de la incertidumbre de los procesos de medición tiene una importancia notoria, ya que es una indicación cuantitativa de la calidad de un resultado de medida y permite evaluar la fiabilidad de este resultado (Fuentes y Sánchez, 2002).
El cálculo de la incertidumbre del método de medición de glucosa en sangre, dependerá de una serie de valores de entrada, que están en función a su proceso de medición, para ello se desarrolla un modelo matemático que identifique y considere tanto las variables de entrada como las de salida (CENAM-em, 2008a, 2008b; Morales et al., 2012); algunas de estas variables o fuentes de incertidumbre significativas que se describen en el modelo matemático, comprenden, la pureza de los reactivos, efectos del analista, el muestreo, efectos de la matriz e interferencias, condiciones ambientales, efectos instrumentales e, incertidumbres de los equipos másicos o volumétricos (EURACHEM/CITAC CG4 et al., 2012); también se consideran aquellas fuentes que no están descritas explícitamente en el modelo, tales como, certificados, manuales, entre otras (CENAM-em, 2008a, 2008b).
El objetivo de esta investigación, desarrollada en el Departamento de Química Biológica y Fisiología Animal, de la Facultad de Ciencias Biológicas, Universidad Nacional Trujillo, fue estimar la incertidumbre de la medición de glucosa en sangre, por el método fotométrico enzimático GOD–PAP.
2. Materiales y Métodos
Material biológico
Muestras de sangre, obtenida de uno de los investigadores.
Reactivos
D (+)- Glucosa anhidro para bioquímica (Merck, 97,5% - 102%), tolerancia en la pureza de ±0,5%. Reactivo de diagnóstico para la determinación cuantitativa in vitro, de glucosa en suero o plasma (Glucosa GOD FS- DIASYS). Agua destilada (conductividad < 3 μmhos/cm).
Equipos
Balanza analítica digital (Sartorius, modelo CP124S), capacidad máxima 120 g y resolución de 0,0001 g.
Micropipeta de volumen variable (Isolab, modelo Laborgeräte GmbH), rango de medición 1 mL a 5 mL.
Termómetro con indicación digital (marca: VWR /TRACEBLE, serie: 111795580) Intervalo de indicación: -50 °C a 70 °C, resolución: 0,1 °C. Espectrofotómetro de uv/vis (ORION, modelo AQUAMATE 8000). Matraz volumétrico (BLAUBRAND, clase A), con volumen nominal de 100 mL.
Diseño experimental
Este trabajo de investigación sigue un estudio descriptivo, retrospectivo de corte longitudinal y diseño no experimental que consistió en la recolección diaria de una muestra de sangre, durante tres días; cada muestra se procesó y analizó por triplicado, dando un total de 9 corridas de ensayo. La precisión del método para la cuantificación de glucosa en sangre, se obtuvo a través del análisis simple de varianza (ANOVA).
Obtención de la muestra
El paciente estuvo en ayunas, aproximadamente 8 horas y, se obtuvo la muestra de sangre, por puntura de la vena cefálica del brazo, con ligadura y sistema de extracción al vacío, sin anticoagulante. Se dejó coagular la sangre durante 15 minutos y se obtuvo el suero por centrifugación a 1500 g durante 15 min.; se aspiró el sobrenadante, con la ayuda de una pipeta Pasteur estéril, se vertió a un vial estéril debidamente etiquetado (Kneip, 2019) y, se determinó la glucosa por el método fotométrico enzimático GOD-PAP. Cada muestra fue analizada por triplicado.
Procesamiento de la muestra para la determinación de glucosa
Para la determinación de glucosa, se ensayaron las muestras de suero, de acuerdo al protocolo Glucosa GOD FS (Diagnostic Systems GmbH [DiaSys], 2015), incluyéndose, además de la muestra y el estándar de glucosa del fabricante, cuatro estándares de glucosa, preparados en el laboratorio y, a las concentraciones de 50 mg/dL, 100 mg/dL , 200 mg/dL y 400 mg/dL , los que sirvieron para la elaboración de la curva de calibración.
Estimación de la incertidumbre en la determinación de glucosa
El proceso de estimación de la incertidumbre se realizó de acuerdo al EURACHEM - Cuantificación de la Incertidumbre en Medidas Analíticas (CITAC), la Directriz para la estimación de la incertidumbre de la medición en laboratorios clínicos (DA-acr-19D)-INACAL versión 00 y, la Guía para la validación y la verificación de los procedimientos de examen cuantitativos empleados por el laboratorio clínico-CENAM.
Especificación del modelo matemático en la determinación de glucosa en sangre
Los modelos matemáticos empleados en la preparación de la disolución madre de glucosa, en la preparación de los estándares de glucosa para la curva de calibración y, en la determinación de la concentración de glucosa en sangre (EURACHEM/CITAC, 2012), se detallan a continuación:
Ecuación utilizada para determinar la concentración de la solución madre de glucosa de 100 mg/100 mL:
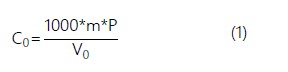
donde, C0: concentración de la solución stock de glucosa (g/L); m: masa del patrón de glucosa de alta pureza (g); P: pureza del patrón de glucosa como fracción en masa; V0: volumen de solución madre de glucosa preparada (mL); 1000: factor de conversión g a mg.
La ecuación utilizada para determinar las concentraciones de los estándares para la curva de calibración, están definidas por:
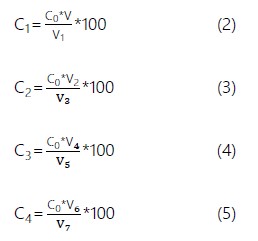
donde, C1: concentración del estándar de calibración 1 de 50 mg/dL; C2: concentración del estándar de calibración 2 de 100 mg/dL; C3: concentración del estándar de calibración 3 de 200 mg/dL; C4: concentración del estándar de calibración 4 de 400 mg/dL; V, V2, V4 y V6: volúmenes de solución madre de glucosa, para preparar los estándares 1, 2, 3 y 4, respectivamente; V1, V3, V5 y V7, los volúmenes finales de cada estándar de calibración.
La ecuación utilizada para determinar la concentración de la glucosa en sangre está determinada por:

donde, Cx: concentración de glucosa en sangre (mg/dL); Ax: Absorbancia media de la solución problema; b0: intercepción de la curva de calibración; b1: pendiente de la curva de calibración (Abs/(mg/dL).
Identificación de las fuentes de incertidumbre
Una vez definido el modelo con sus magnitudes de entrada, se identificaron los componentes de influencia más críticos que impactan en la medición, efectuando un diagrama de causa y efecto (EURACHEM/CITAC, 2012).

Figura 1. Fuentes de incertidumbre en la determinación de glucosa en sangre (método enzimático GOD–PAP).
Cuantificación de la incertidumbre estándar de cada una de la fuentes de incertidumbre.
Estimación de la incertidumbre estándar correspondiente a la concentración de la solución madre de glucosa (C0).
Para la preparación de la solución madre de glucosa, se utilizó una balanza analítica con una precisión de 0,01 mg marca Sartorius (modelo: CP124S). Se pesó la cantidad de 10 g de glucosa anhidra (C6H12O6) de alta pureza, se disolvió y se aforó con agua destilada, en un matraz volumétrico calibrado de 100 mL (V0).
Estimación de la incertidumbre estándar correspondiente a la masa de glucosa.
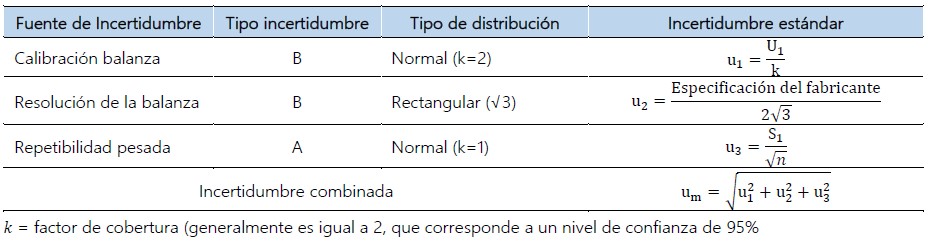
Se estimó, utilizando la incertidumbre expandida de la medición (U1) de la balanza, a través de la ecuación obtenida del certificado de calibración MC-1057-2019 (anexo 1).

Donde
R: Lectura de la balanza después de la calibración, g.
U1: Incertidumbre expandida, g
Esta magnitud tiene 3 fuentes de incertidumbre: calibración, repetibilidad y resolución.
Tabla 01. Incertidumbre combinada correspondiente a la masa de la glucosa.
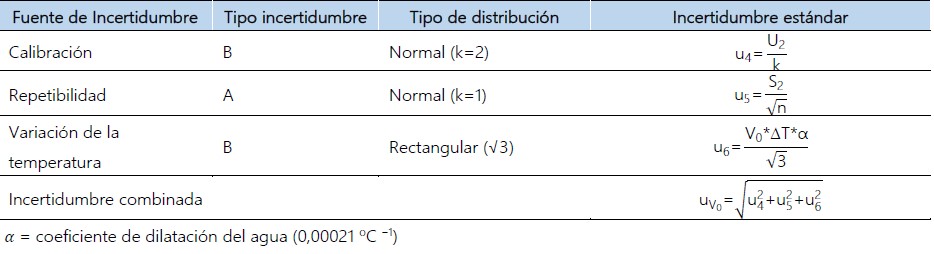
Estimación de la incertidumbre estándar correspondiente al volumen del matraz volumétrico en el que se preparó la solución madre de glucosa (V0).
Esta magnitud tiene 3 fuentes de incertidumbre: la calibración, repetibilidad y variación de la temperatura. Se utilizó un matraz volumétrico de 100 mL cuyo certificado de calibración MV-1841-2019 (anexo 2), reporta una incertidumbre expandida de U2= 0,011 mL. Para la repetibilidad del llenado del material volumétrico se obtuvo la desviación estándar de 10 mediciones de volumen y, la temperatura a la cual se trabajó en el laboratorio fue 23 °C ± 0,1 °C, medido con el termómetro con indicación digital (T-3816-2019), asumiendo una distribución rectangular.
Tabla 02. Incertidumbre combinada correspondiente al volumen del matraz volumétrico utilizado en la preparación de la solución madre de glucosa.
Estimación de la incertidumbre estándar correspondiente a la pureza del reactivo de glucosa.
Esta información, se obtuvo del certificado del proveedor (certificado de análisis del reactivo), como 100% ± 0,5%, Por lo tanto, la pureza de la glucosa es 1,0000 ± 0,0050, para la cual se aplicó una incertidumbre tipo B que sigue una distribución rectangular:
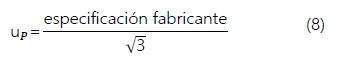
Estimación de la incertidumbre estándar correspondiente a la concentración del estándar 1 de la curva de calibración (C1=50 mg/dL).
Estimación de la incertidumbre estándar correspondiente al volumen tomado de solución madre de glucosa con micropipeta variable de 5 mL (V=1 mL).
Esta magnitud tiene 3 fuentes de incertidumbre: calibración, repetibilidad y variación de la temperatura. Se utilizó una micropipeta de volumen variable de 5 mL cuyo certificado de calibración MV-1851-2019 (anexo 4), reporta que la incertidumbre expandida es: U4= 0,001 mL. Para la repetibilidad del llenado de la micropipeta se obtuvo la desviación estándar de 10 mediciones de volumen y, la temperatura a la cual se trabajó en el laboratorio fue 23,0 °C ± 0,1 °C, medido con el termómetro con indicación digital (T-3813-2019), asumiendo una distribución rectangular.
Tabla 04. Incertidumbre combinada correspondiente a 1 mL, tomado de la solución madre de glucosa con micropipeta variable de 5 mL .

Estimación de la incertidumbre estándar correspondiente al volumen del matraz volumétrico en el que se preparó la solución del estándar de calibración 1 (V1).
Esta magnitud tiene 3 fuentes de incertidumbre: calibración, repetibilidad y variación de la temperatura. Se utilizó un matraz volumétrico de 200 mL cuyo certificado de calibración MV-1840-2019 (anexo 3), reporta una incertidumbre expandida de U3= 0,020 mL. Para la repetibilidad del llenado del material volumétrico se obtuvo la desviación estándar de 10 mediciones de volumen y, la temperatura a la cual se trabajó en el laboratorio fue 23,0 °C ± 0,1 oC, medido con el termómetro con indicación digital (T-3813-2019), asumiendo una distribución rectangular.
Tabla 03. Incertidumbre combinada correspondiente al volumen del matraz volumétrico en el cual se preparó la solución del estándar de calibración 1.

Estimación de la incertidumbre estándar correspondiente a la concentración del estándar 2 de calibración de la curva de calibración (C2=100 mg/dL).
Estimación de la incertidumbre estándar correspondiente al volumen tomado de la solución madre de glucosa con la micropipeta variable de 5 mL (V2=1 mL)
Se utilizó la misma información del punto 2.2.
Tabla 05. Incertidumbre combinada correspondiente a 1 mL, tomado de la solución madre de glucosa con micropipeta variable de 5 mL.
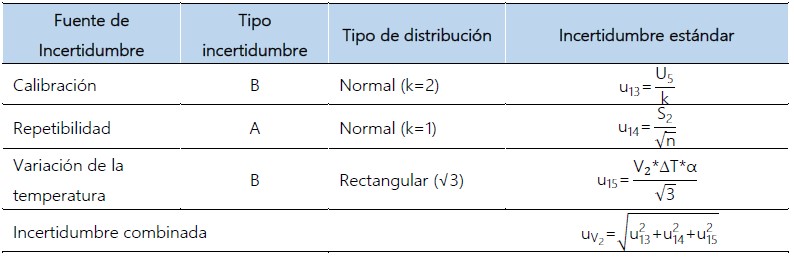
Estimación de la incertidumbre estándar correspondiente al volumen del matraz volumétrico en el que se preparó la solución del estándar de calibración 2 (V3).
Se utilizó la misma información del punto 1.2.
Estimación de la incertidumbre estándar correspondiente a la concentración del estándar 3 de calibración de la curva de calibración (C3=200 mg/dL).
Estimación de la incertidumbre estándar correspondiente al volumen tomado de la solución madre de glucosa con la micropipeta variable de 5 mL (V4=2,00 mL).
Se utilizó la misma información del punto 2.2.
Tabla 06. Incertidumbre combinada correspondiente a 2 mL tomado de la solución madre de glucosa con micropipeta variable de 5 mL.

Estimación de la incertidumbre estándar correspondiente al volumen del matraz volumétrico en el que se preparó la solución del estándar de calibración 3 (V5).
Se utilizó la misma información del punto 1.2.
Estimación de la incertidumbre estándar correspondiente a la concentración del estándar 4 de calibración de la curva de calibración (C4=400 mg/dL).
Estimación de la incertidumbre estándar correspondiente al volumen tomado de solución madre de glucosa con la micropipeta variable de 5 mL (V6=5,00 mL).
Se utilizó la misma información del punto 2.2.; pero considerando una U5 = 0,002 mL, tal como consta en el certificado de calibración (MV-1851-2019).
Tabla 07. Incertidumbre combinada correspondiente a 5 mL tomado de la solución madre de glucosa con micropipeta variable de 5 mL.
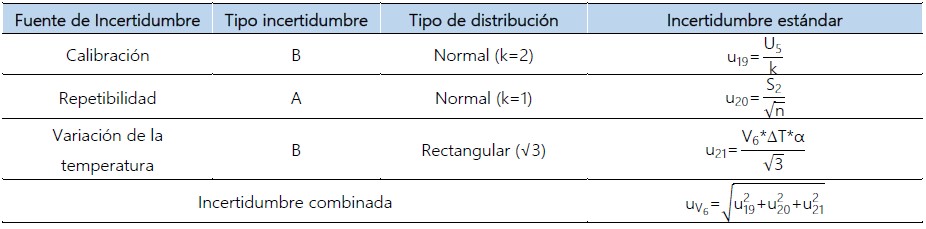
Estimación de la incertidumbre estándar correspondiente al volumen del matraz volumétrico en el que se preparó la solución del estándar de calibración 4 (V7).
Se utilizó la misma información del punto 1.2.
Estimación de la incertidumbre estándar correspondiente a la concentración de la solución problema y del blanco.
Para este caso, se identificaron las siguientes fuentes de incertidumbre: repetibilidad y resolución.
Estimación de la incertidumbre en la medición de la muestra problema (Ax)
Se estimó a través de la variación, en la medición de la absorbancia de la muestra problema, en condiciones de repetibilidad, realizando tres mediciones.
Tabla 08. Incertidumbre combinada correspondiente a la medición de la muestra problema.

Estimación de la incertidumbre en la medición de la solución blanco (Abk)
Se estimó a través de la variación, en la medición de la absorbancia de la solución blanco, en condiciones de repetibilidad, realizando tres mediciones.
Tabla 09. Incertidumbre combinada correspondiente a la medición de la solución blanco.

Estimación de la incertidumbre de la reproducibilidad del método para determinación de glucosa en sangre.
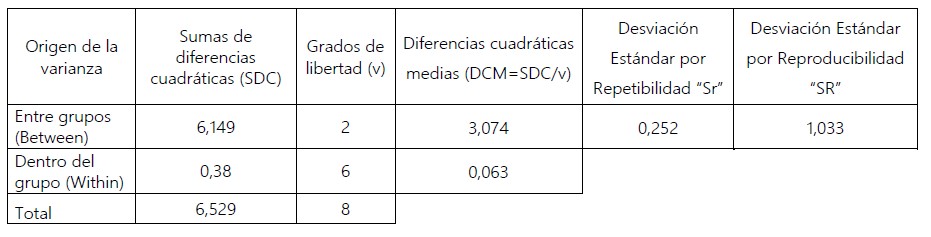
Se determinó la concentración de la glucosa por triplicado durante tres días distintos. Con los datos obtenidos se realizó un tratamiento estadístico ANOVA para el cálculo…de la incertidumbre de la reproducibilidad, obteniéndose el SR de reproducibilidad. Se calculó mediante la ecuación:

Determinación de Incertidumbre Combinada
Una vez que se ha estimado los componentes individuales o los grupos de componentes de la incertidumbre y de expresarlos como incertidumbres estándar, el siguiente paso fue, calcular la incertidumbre combinada usando las tablas que a continuación se presenta
Tabla 10. Estimación de la incertidumbre de reproducibilidad en la concentración de la glucosa.
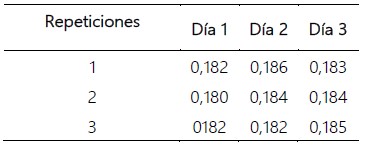
Tabla 11. Estimación de la incertidumbre combinada, asociada a la concentración de la solución madre de glucosa.

Tabla 12. Estimación de la incertidumbre combinada asociada a la concentración del estándar 1 de la curva de calibración (C1=50 mg/dL).

Tabla 13. Estimación de la incertidumbre combinada asociada a la concentración del estándar 2 de la curva de calibración (C2=100 mg/dL).

Tabla 14. Estimación de la incertidumbre combinada asociada a la concentración del estándar 3 de la curva de calibración (C3=200 mg/dL).

Tabla 15. Estimación de la incertidumbre combinada asociada a la concentración del estándar 4 de la curva de calibración (C4=400 mg/dL).

Estimación de Incertidumbre Expandida de la medición (U) de la concentración de glucosa en sangre (Cx)
La incertidumbre expandida provee un intervalo dentro del cual el valor del analito es dado con un alto nivel de confianza. La incertidumbre expandida se obtuvo:

La incertidumbre de la medición de la concentración de glucosa en sangre (Cx), para un factor de cobertura, k = 2 y un nivel de confianza del 95%; se obtuvo mediante la expresión:
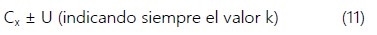
3. Resultados
Las tablas 16, 17, 18, 19, 20 y 21, muestran la incertidumbre combinada correspondiente a la concentración de la solución madre de glucosa, a las concentraciones de las soluciones estándar de calibración y, a la concentración de glucosa en la muestra de sangre, respectivamente. También se aprecia, la incertidumbre estándar de la reproducibilidad del método para la determinación de glucosa en sangre y, la incertidumbre expandida de la medición de la concentración de glucosa en sangre.
Tabla 16. Incertidumbre combinada correspondiente a la concentración de la solución madre de glucosa (C0).
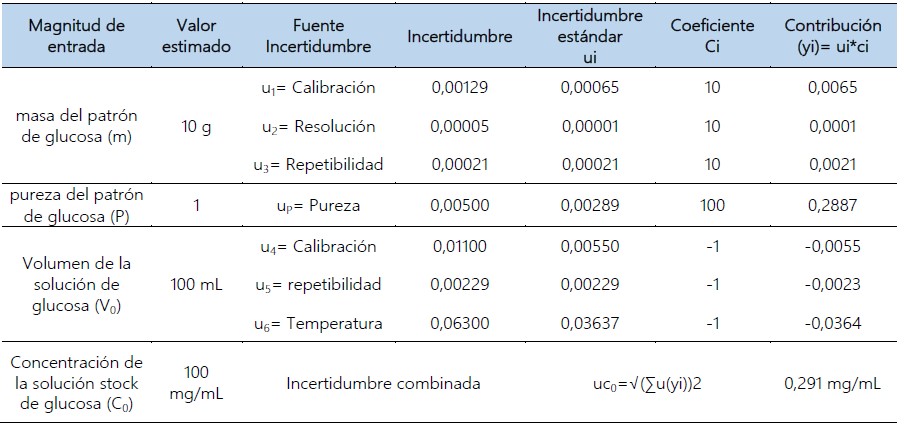
Tabla 17. Incertidumbre combinada correspondiente a la concentración del estándar 1 de calibración.
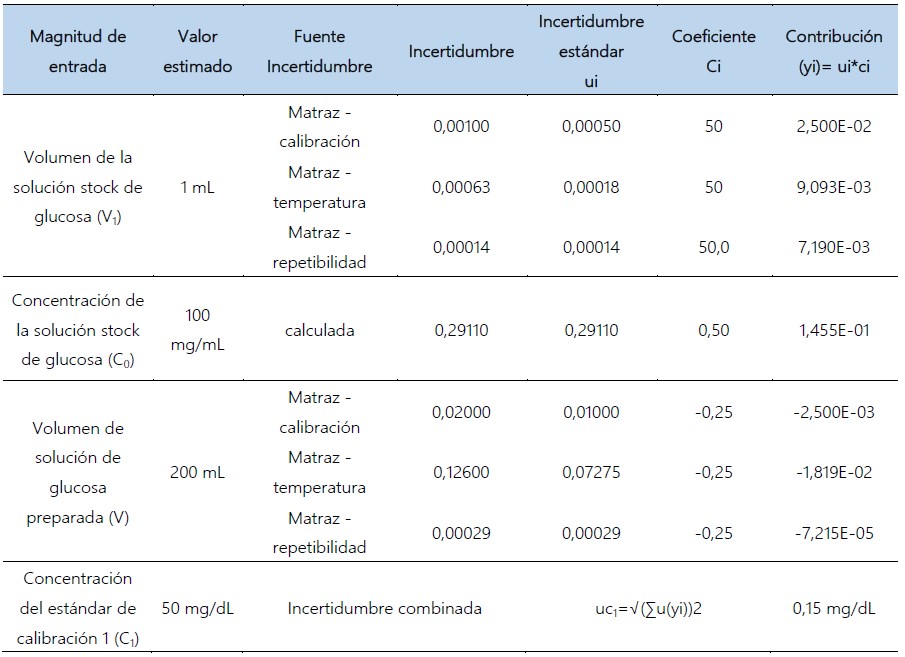
Tabla 18. Incertidumbre combinada correspondiente a la concentración del estándar 2 de calibración.

Tabla 19. Incertidumbre combinada correspondiente a la concentración del estándar 3 de calibración.

Tabla 20. Incertidumbre combinada correspondiente a la concentración del estándar 4 de calibración.

Tabla 21. Incertidumbre combinada correspondiente a la concentración de glucosa en la muestra de sangre (Cx), por el método numérico Kragten. (EURACHEM/CITAC CG4, 2012).

Cálculo de la incertidumbre estándar de la reproducibilidad del método con la ecuación 9 y utilizando la información consignada en los anexos 5 y 6.
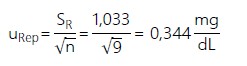
Estimación de la incertidumbre expandida (U)
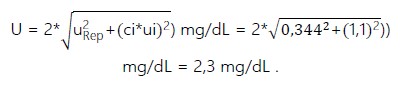
Incertidumbre de la medición de la concentración de glucosa en sangre (Cx)

4. Discusión
En cuanto a la incertidumbre correspondiente a la concentración de la solución madre de glucosa (C0), (tabla 16), se observa que el mayor aporte a la incertidumbre combinada, corresponde a la pureza del reactivo y a la temperatura a la cual se realizó el aforo del matraz volumétrico, este efecto podría disminuirse, empleando un reactivo de alta pureza y, acondicionando la temperatura del ambiente del laboratorio. La incertidumbre combinada fue estimada a través de la ley de propagación de incertidumbres (EURACHEM/CITAC CG4, 2012).
Respecto a la incertidumbre relacionada a la concentración de las soluciones estándar de calibración: C1, C2, C3 y C4, (tablas 17, 18, 19 y 20), se observa que el mayor aporte a la incertidumbre combinada, pertenece a la calibración de la micropipeta, este efecto podría disminuirse, empleando una micropipeta con una menor incertidumbre expandida. La incertidumbre combinada fue estimada a través de la ley de propagación de incertidumbres (EURACHEM/CITAC CG4, 2012).
En la Tabla 21, se muestra las contribuciones a la incertidumbre de la medición para la concentración de glucosa en la muestra de sangre Cx, se aprecia que las fuentes con mayor contribución son: la medición de la muestra y del blanco, este efecto podría disminuir, realizando más repeticiones de la muestra y del blanco.
Se pudo establecer la incertidumbre de la medición para la determinación de glucosa en sangre (método enzimático GOD–PAP) siguiendo la metodología descrita en Quantifying Uncertainty in Analytical Measurement (QUAM) obteniéndose que la incertidumbre expandida relativa, para un nivel de confianza de aproximadamente 95% con k=2, fue de 2,4 % (2,3/95,9*100) en el rango de 50 a 400 mg/dL. Similarmente, Estevinho et al. (2013), reportaron una incertidumbre expandida relativa menor al 10% en el rango de 70,0 a 200,0 mg/dL; según Huang et al. (2005), la incertidumbre para un nivel de confianza de aproximadamente 95% con k=2, es de 4,32 mg/dL a 9,32 mg/dL en el rango de 102,33 mg/dL a 294,65 mg/dL.
Pérez-Castorena y Guevara-Hernández (2002) estimaron para una concentración de glucosa de 4,74 mmol/dL±0,324 mmol/L, una incertidumbre expandida relativa de 6,8% con un factor de cobertura k=2. Por su parte, el Institute for Quality Management in Healthcare [IQMH] (2014) reportó una incertidumbre de la medición de la glucosa plasmática de 6,8 mmo/L±0,4 mmol/L (probabilidad de cobertura del 95%), lo que es equivalente a una incertidumbre expandida relativa de 5,9 %.
Para realizar una adecuada estimación de la incertidumbre de la concentración de glucosa en sangre es necesario conocer las fuentes de error en el método analítico empleado, aplicar conceptos básicos de estadística, disponer de los documentos de calibración de los equipos empleados y definir la metodología a seguir. La estimación de la incertidumbre en mediciones analíticas no sólo sirve para garantizar la calidad de la medición, sino que permite identificar las fuentes de error asociadas a esa medición y cuantificar su contribución; una forma de disminuir la incertidumbre es contar con equipamiento y analistas idóneos (EURACHEM/CITAC CG4, 2012).
5. Conclusiones
La incertidumbre de la medición para la determinación de glucosa en sangre, con un factor de cobertura de k=2 y con un nivel de confianza de aproximadamente 95%, es 2,3 %.
Los factores que contribuyeron, significativamente, a la incertidumbre de la medición para la determinación de glucosa en sangre, fueron: peso de reactivo (pureza) y temperatura del ambiente del laboratorio.
6. Contribución de autores
Todos los autores han participado en la ejecución y la redacción del artículo científico.
7. Conflicto de intereses
Los autores declaran que no existe conflicto de interés.
8. Referencias Bibliográficas
CENAM-em. (2008a). Guía técnica sobre trazabilidad e incertidumbre en las mediciones analíticas que emplea la técnica de titulación volumétrica. Centro Nacional de Metrología, 1-65.
CENAM-em. (2008b). Guía técnica sobre trazabilidad e incertidumbre en las mediciones analíticas que emplean la técnica de espectrofotometría de ultravioleta-visible. Centro Nacional de Metrología, 1-69.
Diagnostic Systems GmbH [DiaSys]. (2015). Glucosa GOD FS. Reactivo de diagnóstico para la determinación cuantitativa In Vitro de glucosa en suero o plasma en equipos fotométricos.
Duxbury, D. (2006). An enzymatic clinical chemistry laboratory experiment incorporating an introduction to mathematical method comparison techniques. Biochemistry and molecular biology education, 32(4), 246–249.
Estevinho, B., Ferraz, A., Santos, L., Rocha, F. & Alves, A. (2013). Uncertainty in the determination of glucose and sucrose in solutions with chitosan by enzymatic methods. Journal of the Brazilian Chemical Society, 24(6), 931-938.
EURACHEM/CITAC CG4. (2012). Cuantificación de la Incertidumbre en Medidas Analíticas. Tercera edición, Editors S L R Ellison (LGC, UK) A Williams (UK).
Fuentes, X. y Sánchez, M. (2002). Guía para estimar la incertidumbre de medida en ciencias de laboratorio clínico. Bioquimia, 27(4), 112-120.
Huang, HC., Chien, CH., Wang, CY., Chong, FC. (2005). Evaluating the uncertainty of measurement on blood's glucose level. Biomed Eng Appl Basis Comm, 17, 31-37.
Institute for Quality Management in Healthcare (IQMH). (2014). Guidance on Measurement Uncertainty for Medical Laboratories.Versión 1.0. Medical L
Kneip, M. (2019). Manual de Toma de Muestras en Laboratorio Clínico. Programa Nacional de Controle de qualidade (PNCQ). 3ra edición.
Martinello, F., Snoj, N., Skitek, M. y Jerin, A. (2019). The top-down approach to measurement uncertainty: which formula should we use in laboratory medicine? Biochemistry Med (Zagreb), 30(2), 1-9.
Milinkovi, N., Ignjatovi, S., Sumarac, Z. y Majkic-Singh, N. (2018). Uncertainty of measurement in laboratory medicine. J Med Biochem, 37(3), 279-288.
Morales, A., Rángel, E., Ramírez, A. y Dorantes, H. (2012). Metodología para el cálculo de la incertidumbre en la determinación de cobre por espectroscopia de absorción atómica. Avances en Ciencias e Ingeniería, 3 (4), 143-155.
Pérez-Castorena, A., Guevara-Hernández, A. (2002). Cálculo de la incertidumbre asociada al resultado de la medición de glucosa. Bioquímica, 27(2), 32-40.
San Román, M. C. (2009). Calibración y control de calidad de instrumentos de análisis clínico. Núcleo de Ingeniería biomédica facultades de medicina e ingeniería, 1-9.
Ventura, S., Chueca, P., Rojo, I. y Castaño, J. L. (2007). Errores relacionados con el laboratorio clínico. Química Clínica, 26 (1), 23-28.
VIM. (2012). Vocabulario Internacional de Metrología Conceptos fundamentales y generales, y términos asociados. 3ª edición. Centro Español de Metrología.
Anexo 1. Certificado de calibración de la balanza analítica.

Anexo 2. Certificado de calibración del matraz volumétrico de 100 mL.

Anexo 3. Certificado de calibración del matraz volumétrico de 200 mL.

Anexo 4. Certificado de calibración de la micropipeta de 5 mL, de volumen variable.
Anexo 5. Concentración de glucosa (mg/dL), para obtener la desviación estándar de la reproducibilidad del método.
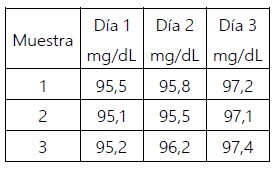
Anexo 6. ANOVA de las concentraciones de glucosa (mg/dL).