Artículo de revisión
COVID19 – Breve revisión del SARS-CoV-2
COVID19 - Brief review of SARS-CoV-2
Anthony Leon 1
1 SARS International Centre for Marine Molecular Biology
Thormøhlens Gate 55, 5008. Bergen. Noruega
*Autor para correspondencia: Anthony.Leon@uib.no
Recibido: 1 de junio, 2020. Aceptado: 29 de junio, 2020
RESUMEN
En diciembre del 2019, una enfermedad respiratoria denominada COVID19 apareció en la ciudad de Wuhan, China, y se expandió a nivel global. Dicha enfermedad es causada por el coronavirus SARS-CoV-2, y constituye la mayor amenaza a la salud pública dentro de las ultimas décadas. Actualmente, es vital estudiar dicha enfermedad a nivel multidisciplinario para encontrar tratamientos efectivos, así como para comprender su desarrollo e impacto dentro de la historia humana. Este artículo de revisión se centra en recapitular la información que se conoce hasta la fecha sobre este virus, su origen, características y las estrategias que diversos gobiernos han adoptado en los últimos meses.
Palabras claves: COVID19, coronavirus, SARS-CoV, SARS-CoV2.
ABSTRACT
In December 2019, a respiratory disease named COVID19 emerged in the city of Wuhan, China, and it spread around the globe. This disease is caused by the SARS-CoV-2 coronavirus and it constitutes the major threat to public health in the last decades. Currently, it is vital to study this disease at a multidisciplinary level in order to find effective treatments, and to understand its development and impact in human history. This review focus on collecting the so-far-known information about this virus, its origin, characteristics and the strategies adopted by several governments in the last months.
Keywords: COVID19, coronavirus, SARS-CoV, SARS-CoV2.
Mensaje clave
La información brindaba en este artículo de revisión está fundamentada en una investigación bibliográfica rápida a partir de artículos citados en Pubmed, así como datos accesibles en NCBI y prensa internacional.
Debido al avance rápido de los estudios sobre SARS-CoV-2, gran parte de la información mundial es actualizada diariamente, por lo cual este artículo puede contener información susceptible al cambio en las siguientes semanas.
DOI: http://dx.doi.org/10.17268/rebiol.2020.40.01.11
1. INTRODUCCIÓN
En diciembre del 2019 se reportó un inusual caso de enfermedad respiratoria en Wuhan, China. Rápidamente, dicha enfermedad se expandió por el mundo, creando alarma y preocupación a nivel global. El patógeno causante de dicha enfermedad fue identificado como un nuevo virus de tipo ARN perteneciente al género Betacoronavirus, el cual se encuentra dentro de la familia Coronaviridae (Guan et al., 2020). Debido a la similitud filogenética de dicho virus con el previamente identificado SARS-CoV (Coronavirus causante de síndrome respiratorio agudo severo), pasó a llamarse SARS-CoV-2. Luego, la enfermedad fue denominada como COVID19 por la Organización Mundial de la Salud (Guan et al., 2020; Castagnoli et al., 2020; WHO, 2020). Actualmente, más de 6,7 millones de personas han sido afectadas por esta enfermedad, causando la muerte de casi 400000 personas en todo el mundo (WHO, 2020) (Figura 1).
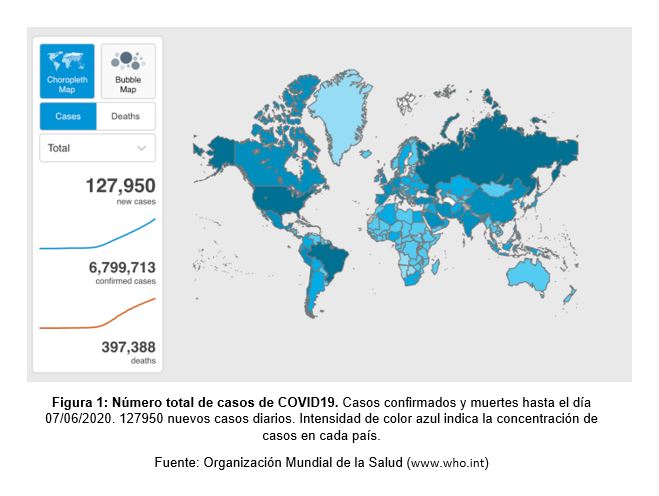
Se ha discutido ampliamente el posible origen de este virus. Sin embargo, no existen estudios definitivos que puedan responder a dicha pregunta. Debido a que esta enfermedad apareció en Wuhan, se relacionó directamente con la comercialización y consumo de animales salvajes en los mercados locales (Guan et al., 2020). A partir de esto, durante los últimos meses se han recopilado diferentes estudios que pretenden dilucidar el origen del SARS-CoV-2, así como su impacto a nivel epidemiológico y posibles tratamientos. En este artículo se discuten las distintas teorías concernientes al origen de dicho virus, las características del virus, los síntomas de la enfermedad y las estrategias médicas y sociales adoptadas en las últimas semanas.
Origen del SARS-CoV-2: ¿Fue un murciélago o un pangolín?
El origen del SARS-CoV-2 es un misterio, sin embargo, diversos estudios genómicos realizados en el este virus determinaron que su secuencia es 96% idéntica a un tipo de coronavirus encontrado en murciélagos. Este virus, denominado RaTG13, fue previamente aislado y reportado en la provincia de Yunnan, China (Forster et al., 2020; Zhang et al., 2020). A pesar de la similitud en su secuencia genómica, RaTG13 posee diferencias importantes con respecto al virus en humanos. Las proteínas “espigas” presente en todos los coronavirus poseen una cavidad llamada dominio de unión al receptor, el cual es vital para que el virus reconozca ciertas moléculas (receptores) en la superficie de las células e ingrese en ellas (receptores ACE2, en el caso de los humanos). Dicho dominio es diferente entre ambos coronavirus, lo que significa que RaTG13 no es capaz de infectar humanos (Cyranoski, 2020). Ya que diversas publicaciones en los últimos años han demostrado una gran incidencia de estos coronavirus en murciélagos, se considera que estos animales constituyen un reservorio natural de esta familia de virus (Cyranoski, 2020).
Otros estudios han permitido identificar coronavirus similares en otros animales, como es el caso del pangolín. De hecho, el virus Pangolin-CoV es 91% idéntico a SARS-CoV-2, y es el segundo más cercano filogenéticamente a este virus, después del RaTG13 (Zhang et al., 2020) (Figura 2). Sin embargo, este virus si posee un dominio de unión al receptor, casi idéntico con el de humanos (Cyranoski, 2020). Estudios previos identificaron diversas poblaciones de pangolines infectados con este virus. De hecho, Liu et al. (2019), reportaron en diciembre 21 pangolines que fueron recuperados en malas condiciones dentro de una reserva natural, de los cuales 16 murieron. Todos los animales que murieron presentaban fibrosis pulmonar, y algunos también presentaban hepatomegalia y esplenomegalia (Liu et al., 2019). Estos síntomas son comunes en personas que desarrollan COVID19 y sugieren similitud en las patologías causadas por ambos virus.
Lo único seguro es que el SARS-CoV-2, o un ancestro muy similar, estuvo escondido en alguno de estos animales durante décadas. De hecho, se cree que la línea que dio origen al actual coronavirus pudo divergir del Pangolin-CoV hace unos 140 años. Luego, hace 40-70 años, dicho ancestro se separó del coronavirus en murciélagos (el cual perdió su dominio de unión a receptores humanos).
Esta hipótesis sugiere una larga historia evolutiva dentro de los murciélagos y pangolines, y que el virus aún se encuentra presente dentro de estos “reservorios naturales” (Cyranoski, 2020).
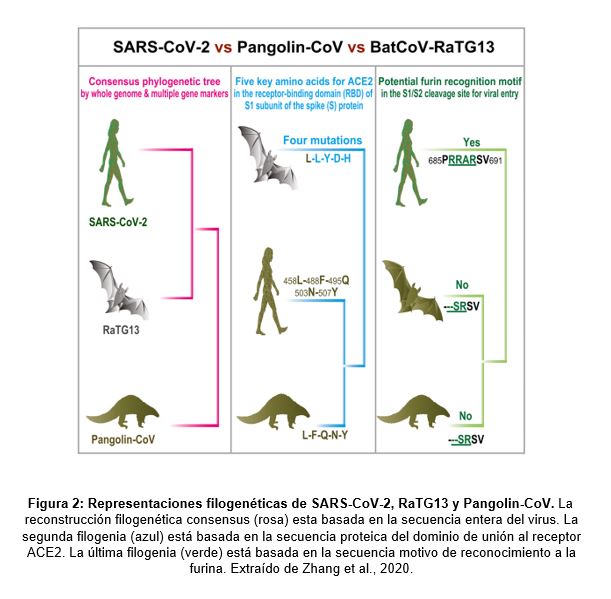
Características del SARS-CoV-2
Luego de la aparición del SARS-CoV en el 2003, el brote actual del SARS-CoV-2 ha permitido estudiar como el virus ha evolucionado y ha desarrollado diversas adaptaciones que le han conferido mayor letalidad. A diferencia de otros virus cercanos, el SARS-CoV-2 ataca fácilmente las células humanas a diferentes niveles: primero en los pulmones y garganta, y una vez dentro, el virus hace uso de un arsenal de moléculas que atacaran diversos órganos (Cyranoski, 2020).
SARS-CoV-2 tiene aproximadamente 125nm de diámetro, y es grande en comparación a otros virus de tipo ARN. De hecho, su genoma consta de 30000 bases y codifica 29 proteínas (Figura 3), lo que le convierte en el virus ARN con el genoma más largo (3 veces más grande que el virus del VIH y de la Hepatitis C; y 2 veces más grande que el virus de la influenza) (Kim et al., 2020; Cyranoski, 2020).
Los coronavirus también se encuentran entre los pocos virus ARN que cuentan con un mecanismo de corrección genómica, el cual les impide acumular mutaciones no ventajosas. Por tal motivo, algunas drogas como la ribavirina (la cual induce mutaciones) es ineficaz contra este virus. De hecho, las mutaciones pueden tanto beneficiar como favorecer a los virus. En el caso de la influenza, esta muta 3 veces más rápido que los coronavirus, y esto le permite evolucionar más rápido (Cyranoski, 2020).
Sin embargo, los coronavirus son capaces de recombinarse frecuentemente al intercambiar parte de su ARN con otros coronavirus. Es decir que, cuando dos coronavirus distantes se logran encontrar dentro de la misma célula, pueden recombinarse y crear nuevas versiones capaces de infectar nuevos tipos celulares, e incluso saltar a otras especies. Esto es lo que sucede a menudo en los murciélagos, los cuales acarrean 61 virus capaces de infectar a los humanos. De hecho, se sabe que los tres coronavirus que han ocasionado enfermedades respiratorias a nivel mundial (SARS-CoV, SARS-CoV-2 y MERS-CoV) provienen de murciélagos (Cyranoski, 2020).
Para infectar las células, el coronavirus usa una proteína en forma de punta que sobresalen de su superficie y se acopla a la membrana celular. Los análisis genómicos de este nuevo coronavirus han revelado que dichas proteínas, conocidas como “espigas”, poseen un sitio de activación que es reconocido por una enzima llamada furina. Esto es significante porque la furina se encuentra en muchos tejidos humanos, incluyendo los pulmones, hígado e intestino delgado; lo que significa que el virus tiene el potencial para atacar múltiples órganos (Mallapaty, 2020).
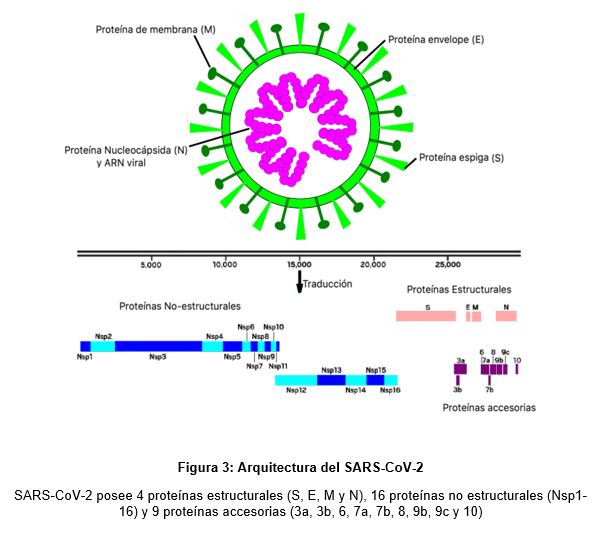
Síntomas del COVID19
Los síntomas principales que se presentan en esta enfermedad son complicaciones en las vías respiratorias y desarrollo de fibrosis pulmonar en pacientes de riesgo (Ledford, 2020). Los pacientes pueden experimentar al inicio síntomas en la nariz o en la garganta, produciendo tos y una disrupción entre sabor y olfato, y la sintomatología puede terminar ahí; o puede bajar hasta los pulmones y dañarlos. La forma como llega ahí, sea moviéndose de célula a célula, o por medio de fluidos, es desconocida. Sin embargo, si llega al pulmón, se produce una neumonía (Cyranoski, 2020).
La habilidad del SARS-CoV-2 para infectar y reproducirse rápidamente en la parte alta del sistema respiratorio fue sorpresivo para los investigadores, ya que el SARS-CoV no tiene dicha capacidad.
De hecho, en el caso del COVID19, las partículas virales son capaces de pasar de la garganta a la saliva (contagiando a otras personas) incluso antes de que los síntomas empiecen. Además, se sabe que el SARS-CoV-2 posee un dominio de unión al receptor ACE2 que es 10-20 veces más eficaz que el presente en el SARS-CoV. Estas características hacen que el nuevo SARS-CoV-2 sea mucho más efectivo infectando personas que el SARS-CoV (Cyranoski, 2020). Sin embargo, a pesar del gran número de fatalidades asociadas al COVID19, el riesgo de muerte parece ser menor que al del SARS-CoV o del MERS-CoV (Guan et al., 2020; Lu et al., 2020), los cuales también se transmiten por medio del aire y afectan las vías respiratorias.
A nivel pulmonar, todos estos coronavirus infectan y destruyen la barrera celular que separa a los alveolos pulmonares de los capilares, haciendo que el líquido dentro de los alveolos fugue y bloquee el paso de oxígeno hacia la sangre. En adición a esto, otras células, como los macrófagos, también bloquean las vías respiratorias al mismo tiempo (Cyranoski, 2020). Un buen sistema inmune puede limpiar esto, pero un sistema sobre activado puede crear daño tisular si la inflamación es muy severa.
Si este es el caso, los pulmones nunca se recuperan y la persona muere (Cyranoski, 2020).
A pesar de toda la información recopilada, no se sabe exactamente si la letalidad proviene del virus en sí mismo, o de la respuesta del sistema inmune, el cual sobrecarga los órganos del paciente y esto dificulta que los médicos determinen la mejor forma para tratar a las personas infectadas. De hecho, diversos datos clínicos sugieren que el sistema inmune juega gran parte en el declive y muerte de las personas diagnosticas con COVID19. Es decir, luego que el virus afecta a los pulmones, se producen niveles elevados de citoquinas en la sangre que aumentan la respuesta inmune. Dicha respuesta depende de una pequeña pero potente proteína de señalización llamada interleucina-6 (IL-6). Esta proteína atrae algunos componentes del sistema inmune, como los macrófagos, los cuales aumentan la inflamación y son capaces de dañar las células normales del pulmón (Ledford,2020). Por tales razones, ciertos tratamientos contra esta enfermedad están dirigidos a suprimir la respuesta inmune (como el uso de esteroides), sin embargo, esto puede disminuir la capacidad del cuerpo para monitorear la infección. La estrategia ideal sería entonces usar una droga que bloquee la actividad de la IL-6 y reduzca el flujo de macrófagos hacia los pulmones. Dichas drogas (inhibidores de IL-6) ya existen, y son usadas frecuentemente en el tratamiento de artritis reumatoide y otros desordenes (Ledford,2020).
Todas estas características convierten al COVID19 en una enfermedad altamente contagiosa, sino también de difícil tratamiento al afectar ampliamente al sistema inmune, ya que los pacientes no solo presentan daños directos en las vías respiratorias, sino que otros daños (como los causados por el exceso de citoquinas) generan fallas en diversos tejidos y órganos como el intestino, corazón, sangre, esperma, ojos y posiblemente el cerebro (Cyranoski, 2020).
Estrategias adoptadas contra el COVID19
Clásicamente, se cree que las enfermedades virales que afectan a las vías respiratorias requieren tener agentes infecciosos muy pequeños (< 5um) ya que las partículas más grandes sedimentan y no permanecen en el aire. Sin embargo, muchas de estas enfermedades respiratorias también se pueden transmitir por contacto cutáneo, o ventilación en ciertas circunstancias (por ventilación artificial o entubamiento en hospitales). Con respecto al brote del SARS-CoV-2, se discutió por mucho tiempo si el virus podía transmitirse por medio del aire y que medidas de precaución se deben tomar en cuenta para evitar su propagación (Seto, 2015).
La primera medida sugerida por la OMS, y adoptada por diversos países fue el distanciamiento social, el cual consta de evitar las aglomeraciones de personas y en mantener 2 metros de distancia entre ellas. Esta sugerencia se basa en la premisa que el SARS-CoV-2, al ser un virus grande y pesado, no puede mantenerse en el aire y sedimenta a menos de 2 metros luego de su expulsión por las vías respiratorias. La reacción rápida, cuarentena y medidas de distanciamiento social (como el cierre de escuelas y negocios) han ayudado a reducir la transmisión del virus en diversos países.
Actualmente se estudia la efectividad de las medidas adoptadas por diferentes gobiernos para predecir las tasas de trasmisión e infección en sus regiones. Esta información será vital para que dichos gobiernos puedan diseñar estrategias que permitan regresar a la población a las actividades normales y evitar olas secundarias de infección (Gibney, 2020). La plataforma puesta en servicio por la OMS recolecta la información de diversos países y centros de investigación con la final de estandarizar esta información y permitir su comprensión a nivel global (Gibney, 2020; WHO, 2020).
En el caso del continente americano, las malas decisiones tomadas por algunos gobernantes han disparado el número de casos durante los últimos dos meses (Figura 4). Países como Estados Unidos y Brasil presentan actualmente el mayor número de contagios en sus respectivas regiones, y este número aumenta día a día. A diferencia de América, en Europa se ha alcanzado una curva mas plana, en la cual el número de contagios es estable y ha empezado a disminuir. Dicho contexto ha permitido que diversos países retomen las actividades laborales, resguardando aún su salud publica.
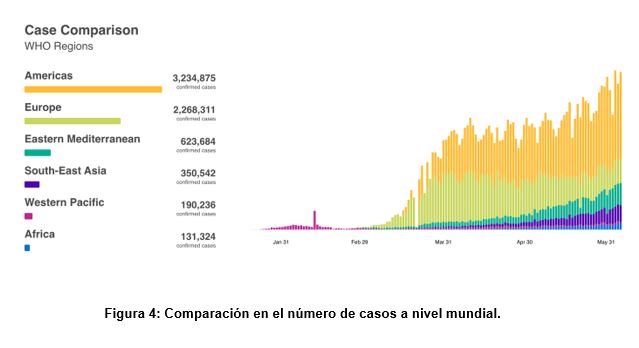

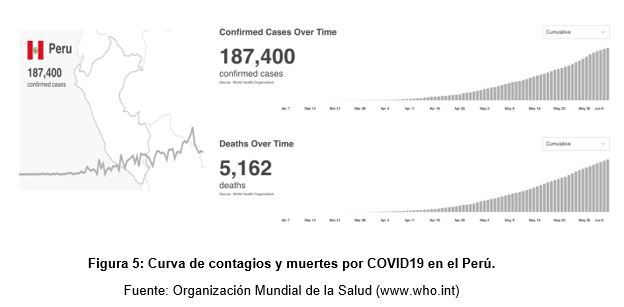
La situación no es muy diferente en el Perú, ya que el numero de casos ha aumentado de manera uniforme en las últimas semanas (Figura 5). Actualmente se han registrado más de 187000 casos (5000 de los cuales han terminado en deceso), ocupado el 8vo lugar a nivel mundial de contagios totales, después de Italia (WHO, 2020; Worldometers). El hecho que la cantidad de contagios en nuestro país haya aumentado drásticamente sugiere una mala administración y mal manejo de la pandemia a nivel nacional. A pesar de que el Perú fue uno de los primeros países de América del Sur en adoptar medidas preventivas estrictas, la respuesta de la población no ha cumplido la expectativa que corresponde frente a una pandemia mundial. Esto se evidencia al comparar la cantidad de casos con países vecinos como Chile y Argentina, en los cuales las medidas de prevención fueron tomadas al mismo tiempo que en el Perú.
Mientras que las personas infectadas inundan los hospitales y el sistema de salud colapsa, los médicos alrededor del mundo tratan de manejar y comprender grandes cantidades de datos incompletos con respecto al COVID19, con la finalidad de encontrar la forma de ayudar a sus pacientes (Ledford, 2020). Diariamente se realizan pruebas clínicas de vacunas experimentales contra el virus, pero a pesar que los esfuerzos para crear una vacuna viable, no se cree que esta pueda estar lista hasta dentro de unos 12 meses aproximadamente (Ledford, 2020). De hecho, más de 90 vacunas se están desarrollando por diversos equipos de investigación y universidades alrededor del mundo. Los investigadores ponen a prueba diferentes tecnologías en la producción de vacunas experimentales y han comenzado inyectándolas en voluntarios; mientras que otros han empezado probándolas en animales (Callaway, 2020). Por lo menos 7 equipos están desarrollando vacunas usando el mismo virus en una forma inactivada o más débil (como aquellas contra el sarampión y el polio), pero estas requieren extensivas pruebas de seguridad antes de ser comercializadas. Por ahora, Sinovac Biotech en Beijing ya ha empezado a probar una versión inactiva del SARS-CoV-2 en humanos (Callaway, 2020).
Sin expectativas de que el coronavirus se aleje, los investigadores buscan modelos animales que permitan entender mejor al virus. Modelos como ratones; monos y hurones son usados para responder preguntas claves sobre la enfermedad, así como el uso de drogas potenciales y vacunas.
Diversos laboratorios en China ya han presentado resultados provenientes de estudios en donde se infectaron monos y ratones previamente diseñados para ser susceptibles al SARS-CoV-2. De la misma forma, equipos de investigación en Geelong, Australia, también estudian dicha infección en hurones, los cuales son modelos muy populares en el estudio de infecciones respiratorias, ya que la fisiología de sus pulmones es similar a la de los humanos (Cohen, 2020)
Sin embargo, ningún animal es perfecto, y se necesitan varios modelos para estudiar este virus. Por ejemplo, experimentos en primates infectados con COVID19 han demostrado que los macacos Rhesus desarrollan esta enfermedad levemente. Ninguno de estos primates desarrollo fiebre, sin embargo, los rayos X en sus pulmones mostraron signos de neumonía similar a los humanos. El hecho de que los monos desarrollen síntomas leves, similares a aquellos en humanos, es un paso importante. No obstante, es necesario encontrar y/o desarrollar modelos que desarrollen infecciones severas (Cohen, 2020).
En este contexto, no solo los hospitales, sino también los laboratorios alrededor del mundo están colapsando. Los investigadores han debido detener las investigaciones y pruebas clínicas de otras enfermedades, con la finalidad de abordar esta pandemia. Algunos médicos, incluso, prueban diferentes tratamientos “no aprobados”, en un último esfuerzo para salvar vidas. Por ejemplo, algunos hospitales en New York intentan usar el plasma proveniente de personas que se han recuperado del COVID19, para tratar personas enfermas. Una ventaja clave de esta técnica es que el plasma se encuentra disponible inmediatamente, mientras que las drogas y vacunas toman meses o años en ser desarrolladas. Los investigadores esperan que esta antigua técnica de infundir pacientes con los anticuerpos provenientes de otras personas sea efectiva. Estos esfuerzos son también similares a los realizados en China, donde se infundio plasma en pacientes. Sin embargo, aún no se han obtenido resultados concretos hasta la fecha (Maxmen, 2020; Cohen, 2020).
2. CONCLUSIONES
La comunidad científica y médica se ha esforzado en entender la naturaleza del SARS-CoV-2 durante los últimos meses, y ha luchado en contener el paso de esta enfermedad en casi todas las naciones del mundo. A pesar de los esfuerzos, aún no es posible controlar el avance de esta pandemia, y tampoco se ha logrado obtener un tratamiento efectivo contra ella. El origen de este nuevo coronavirus también es un misterio, sin embargo, existen pruebas que sugieren un origen zoonótico, que involucra tanto a murciélagos como a pangolines, en China. Las costumbres alimenticias en esta región probablemente facilitaron el salto de este virus al ser humano. Esto, sumado a la poca organización política y social a nivel mundial, ha influenciado la diseminación del virus en todos los países. Dentro del contexto histórico, esta pandemia marca un antes y un después en la salud pública mundial, que esperamos pueda ser tomada con responsabilidad y como ejemplo frente a futuras crisis sanitarias.
3. REFERENCIAS BIBLIOGRÁFICAS
Castagnoli, Riccardo, Martina Votto, Amelia Licari, Ilaria Brambilla, Raffaele Bruno, Stefano Perlini, Francesca Rovida, Fausto Baldanti, and Gian Luigi Marseglia. “Severe Acute Respiratory Syndrome Coronavirus 2 (SARS-CoV-2) Infection in Children and Adolescents: A Systematic Review.” JAMA Pediatrics, April 22, 2020. https://doi.org/10.1001/jamapediatrics.2020.1467.
Callaway, E. (2020). The race for coronavirus vaccines: a graphical guide. Nature, 580(7805), 576-577. https://doi.org/10.1038/d41586-020-01221-y
Cohen, Jon. “Mice, Hamsters, Ferrets, Monkeys. Which Lab Animals Can Help Defeat the New Coronavirus?” Science | AAAS, April 13, 2020 https://doi:10.1126/science.abc2335
Cyranoski, David. “Profile of a Killer: The Complex Biology Powering the Coronavirus Pandemic.” Nature 581, no. 7806 (May 4, 2020): 22–26. https://doi.org/10.1038/d41586-020-01315-7.
Cyranoski, David. “Mystery Deepens over Animal Source of Coronavirus.” Nature 579, no. 7797 (February 26, 2020): 18–19. https://doi.org/10.1038/d41586-020-00548-w.
Forster, Peter, Lucy Forster, Colin Renfrew, and Michael Forster. “Phylogenetic Network Analysis of SARS-CoV-2 Genomes.” Proceedings of the National Academy of Sciences 117, no. 17 (April 28, 2020): 9241–43. https://doi.org/10.1073/pnas.2004999117.
Gibney, Elizabeth. “Whose Coronavirus Strategy Worked Best? Scientists Hunt Most Effective Policies.” Nature 581, no. 7806 (April 27, 2020): 15–16. https://doi.org/10.1038/d41586-020-01248-1.
Guan, Wei-jie, Zheng-yi Ni, Yu Hu, Wen-hua Liang, Chun-quan Ou, Jian-xing He, Lei Liu, et al. “Clinical Characteristics of Coronavirus Disease 2019 in China.” New England Journal of Medicine, February 28, 2020. https://doi.org/10.1056/NEJMoa2002032.
Kim, Dongwan, Joo-Yeon Lee, Jeong-Sun Yang, Jun Won Kim, V. Narry Kim, and Hyeshik Chang. “The Architecture of SARS-CoV-2 Transcriptome.” BioRxiv, March 15, 2020, 2020.03.12.988865. https://doi.org/10.1101/2020.03.12.988865.
Ledford, Heidi. “How Does COVID-19 Kill? Uncertainty Is Hampering Doctors’ Ability to Choose Treatments.” Nature 580, no. 7803 (April 9, 2020): 311–12. https://doi.org/10.1038/d41586-020-01056-7.
Ledford, Heidi. “Coronavirus Shuts down Trials of Drugs for Multiple Other Diseases.” Nature 580, no. 7801 (2020): 15–16. https://doi.org/10.1038/d41586-020-00889-6.
Liu, Ping, Wu Chen, and Jin-Ping Chen. “Viral Metagenomics Revealed Sendai Virus and Coronavirus Infection of Malayan Pangolins (Manis Javanica).” Viruses 11, no. 11 (November 2019): 979. https://doi.org/10.3390/v11110979.
Lu, Roujian, Xiang Zhao, Juan Li, Peihua Niu, Bo Yang, Honglong Wu, Wenling Wang, et al. “Genomic Characterisation and Epidemiology of 2019 Novel Coronavirus: Implications for Virus Origins and Receptor Binding.” Lancet (London, England) 395, no. 10224 (2020): 565–74. https://doi.org/10.1016/S0140-6736(20)30251-8.
Mallapaty, Smriti. “Why Does the Coronavirus Spread so Easily between People?” Nature 579, no. 7798 (2020): 183. https://doi.org/10.1038/d41586-020-00660-x.
Maxmen, Amy. “How Blood from Coronavirus Survivors Might Save Lives.” Nature 580, no. 7801 (March 24, 2020): 16–17. https://doi.org/10.1038/d41586-020-00895-8.
Seto WH. Airborne transmission and precautions: facts and myths. J Hosp Infect. 2015; 89(4):225-8. doi: 10.1016/j.jhin.2014.11.005. PMID: 25578684
Zhang, Tao, Qunfu Wu, and Zhigang Zhang. “Probable Pangolin Origin of SARS-CoV-2 Associated with the COVID-19 Outbreak.” Current Biology: CB 30, no. 7 (06 2020): 1346-1351.e2. https://doi.org/10.1016/j.cub.2020.03.022.
World Health Organization. Coronavirus disease (COVID-19) outbreak. htt://www.who.int
Worldometers: COVID-19 pandemic. https://www.worldometers.info/coronavirus/#countries