1. Introducción
La nanoencapsulación es una tecnología emergente que permite la incorporación de compuestos bioactivos en sistemas de liberación a escala nanométrica, empleando materiales poliméricos o lipídicos. Esta técnica no solo ofrece protección a los compuestos sensibles frente a factores ambientales adversos, sino que también incrementa su biodisponibilidad y posibilita una liberación controlada y dirigida (Torres, 2023). Gracias a estas propiedades, la nanoencap-sulación ha revolucionado el diseño de alimentos funcionales en la industria alimentaria, facilitando la incorporación eficaz de ingredientes con propiedades fisiológicas beneficiosas (Robayo, 2024). En este marco, los compuestos bioactivos de origen vegetal, como los flavonoides, compuestos fenólicos, carotenoides y vitaminas, han despertado un interés creciente debido a su capacidad para contribuir a la prevención de enfermedades crónicas relacionadas con el estrés oxidativo (Jia et al., 2024). Estos compuestos han adquirido relevancia en la nutrición moderna por su potencial para mejorar la salud de las poblaciones que siguen dietas basadas en alimentos vegetales, los cuales los contienen de forma natural (Urrialde et al., 2022).
Particularmente, las plantas medicinales tradicionalmente infravaluadas representan una fuente rica y diversa de estos compuestos bioactivos, muchas veces aún no suficientemente explorados ni aprovechados a nivel industrial. A pesar de su potencial, varios de estos ingredientes presentan limitaciones como baja solubilidad, escasa estabilidad o baja biodisponibilidad, obstáculos que dificultan su incorporación directa en productos alimentarios o nutracéuticos. En este contexto, la nanoencapsulación surge como una estrategia prometedora para superar dichas barreras tecnológicas y promover un uso más sostenible e innovador de plantas medicinales infravaloradas.
El objetivo de esta revisión es explorar el estado del arte en la nanoencapsulación de compuestos bioactivos derivados de plantas poco valorizadas, mediante un enfoque narrativo y bibliométrico. Se analizaron tanto los avances científicos como las tendencias actuales de investigación, con el fin de identificar oportunidades, desafíos y perspectivas futuras en este campo emergente.
2. Fundamentos de la Nanoencapsulación
La nanoencapsulación es una tecnología emer-gente que permite incorporar compuestos bioac-tivos dentro de una matriz o cubierta diseñada a escala nanométrica, con el fin de protegerlos, estabilizarlos y optimizar su acción biológica. Este sistema se basa en la formación de un núcleo que contiene el principio activo y una pared o matriz que lo rodea, cuyos diámetros pueden oscilar entre 1 y 1000 nm; sin embargo, para aplicaciones alimentarias y biomédicas, los tamaños más eficientes suelen situarse entre 50 y 300 nm, rango que favorece la estabilidad coloidal, la difusión controlada y la interacción celular (McClements, 2015). Este confinamiento nanométrico permite resguardar los compuestos sensibles frente a condiciones ambientales adversas como la exposición a la luz, el oxígeno, la humedad o variaciones extremas de pH mejorando así su estabilidad durante el procesamiento y almacenamiento. De igual forma, el tamaño reducido incrementa la solubilidad en medios acuosos y posibilita una liberación dirigida, lo que se traduce en una mayor biodisponibilidad del bioactivo encapsulado.
De acuerdo con Pateiro et al. (2021), la nanoencapsulación no solo prolonga la vida útil y estabilidad química de los compuestos bioactivos, sino que también permite modular su liberación en regiones fisiológicas específicas. Este comporta-miento se logra mediante el diseño de nanopartí-culas con respuestas controladas ante estímulos ambientales o biológicos, tales como variaciones de pH, temperatura o la presencia de enzimas propias del sitio de acción. La reducción del tamaño de partícula a la nanoescala también mejora la interacción con las membranas celulares, promoviendo una absorción más eficiente y, en consecuencia, una mayor efectividad funcional.
Asimismo, Kamble et al. (2025) destacan que el confinamiento de los bioactivos dentro de matrices nanoestructuradas actúa como una barrera física que limita la exposición a factores degradativos durante el procesamiento y alma-cenamiento de alimentos. Esta protección estruc-tural contribuye a preservar la integridad química del compuesto, mejorar su retención y, en muchos casos, potenciar su biodisponibilidad gracias a su capacidad para atravesar la membrana celular mediante procesos de transporte pasivo o mecanismos de absorción especializados. En conjunto, estos aspectos convierten a la nanoencapsulación en una estrategia altamente eficiente para la entrega controlada y protección de compuestos funcionales en sistemas alimentarios y biomédicos.
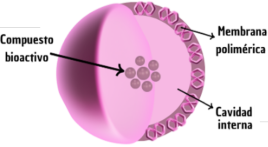
Figura 1. Esquema simplificado de un sistema núcleo-capa.
Figure 1. Simplified diagram of a kernel-shell system.
2.1. Tipo de Nano-vehículos
Para lograr una nanoencapsulación eficaz, se emplean distintos tipos de nanovehículos, cuya selección depende tanto de la naturaleza del compuesto bioactivo como del objetivo funcional y del entorno de aplicación (Norkaew et al., 2019). Entre los sistemas más utilizados destacan los lipídicos, poliméricos (naturales y sintéticos) y metálicos, cada uno con características que los hacen especialmente adecuados para aplica-ciones concretas. Por ello, la Tabla 1 presenta las principales familias de sistemas nanoencapsu-lados, junto con los materiales más empleados. Este análisis evidencia la diversidad de alternativas disponibles, cada una con ventajas específicas en términos de estabilidad, funcionalidad y biocompatibilidad.
2.2. Técnicas de preparación
La producción de estos sistemas de nano encapsulación puede llevarse a cabo mediante diversas técnicas, las cuales pueden ser organizadas en categorías como los métodos químicos, fisicoquímicos y físico-mecánicos, según el principio que utilizan para formar las nanoestructuras.
La técnica seleccionada influye de manera decisiva en aspectos clave como la eficiencia del encapsulado, el tamaño de partícula y el perfil de liberación controlada del principio activo. En este sentido, la Tabla 2 presenta las principales técnicas empleadas, agrupadas según su método y destacando el principio de funcionamiento de cada una. De esta forma, la elección combinada de nanovehículos y técnicas de preparación permite diseñar sistemas de liberación dirigidos que responden de manera específica a las características del compuesto encapsulado y a su aplicación industrial.
Estas características convierten a la nanoencapsulación en una herramienta versátil y eficaz, aplicable en campos tan diversos como la industria alimentaria, farmacéutica y cosmética. En este sentido, la Figura 2 sintetiza las princi-pales aplicaciones industriales de los sistemas nanoencapsulados, destacando su potencial para enriquecer alimentos funcionales, mejorar la eficacia de fármacos y potenciar las propiedades de productos cosméticos. Este esquema ayuda a visualizar cómo el desarrollo de sistemas de liberación controlada impacta directamente en el diseño de productos de consumo con mayor valor añadido y funcionalidad.
5. Desafíos y perspectivas futuras
5.1. Desafíos tecnológicos y científicos
La nanotecnología a adquirido un creciente protagonismo en la ciencia de los alimentos, especialmente mediante la nanoencapsulación de compuestos bioactivos, los cuales suelen presentar baja absorción en el organismo. Los sistemas nanoestructurados contribuyen a mejorar su protección, solubilidad, estabilidad y biodisponibilidad. No obstante, su desarrollo implica retos importantes, como seleccionar el método de obtención adecuado y el nanomaterial más compatible. También es fundamental evaluar su seguridad, por lo que se promueve la regulación toxicológica y el uso de métodos sostenibles como la síntesis ecológica (Bazana et al., 2019).
5.2. Barreras regulatorias y de seguridad
La ausencia de normativas claras sobre nanotecnología ha impulsado el uso de mecanismos voluntarios o regulación blanda, como registros, etiquetado, códigos de conducta, guías y normas técnicas. Estos buscan orientar el uso seguro de nanomateriales mientras se avanza hacia una armonización normativa. Organismos como la ISO, a través del comité ISO/TC-229, y la OCDE, mediante el WPMN, han desempeñado un papel clave en el desarrollo de estándares internacionales. Sin embargo, aún persiste el debate sobre cuál es el enfoque regulatorio más adecuado para una tecnología emergente con múltiples aplicaciones y riesgos aún inciertos (Saldívar Tanaka, 2020).
5.3. Aceptación del consumidor y percepción pública
A pesar del potencial de la nanotecnología, su aceptación por parte del consumidor enfrenta barreras significativas debido al limitado conocimiento que existe sobre ella, lo que puede provocar percepciones divididas en cuanto a su seguridad.
Este desconocimiento puede influir negativa-mente en la disposición del público a aceptar productos que incorporen nanotecnología. Por ello, es esencial promover el diálogo entre la sociedad, los científicos, las autoridades y la industria para fortalecer la confianza y facilitar una adopción informada. Aunque se ha iniciado el debate sobre la percepción pública tanto en países desarrollados como en desarrollo, aún no se han realizado análisis comparativos entre ambos contextos, lo cual limita el diseño de estrategias efectivas de comunicación y educación adaptadas a distintas realidades socioeconómicas (Rathore & Mahesh, 2021).
5.4. Sostenibilidad e innovación futura
La impresión 3D, como técnica de fabricación aditiva, permite construir objetos capa por capa, ofreciendo un control preciso sobre la estructura y propiedades de los materiales. Su aplicación en el ámbito de los nanocompuestos abre nuevas posibilidades para fabricar sistemas de liberación controlada personalizados y con estructuras específicas que optimicen la funcionalidad de los compuestos bioactivos encapsulados (Tzounis & Bangeas, 2022).
Este enfoque no solo puede mejorar la eficiencia de los nanoencapsulados, sino también reducir el desperdicio de materiales y facilitar la fabricación descentralizada de ingredientes funcionales o componentes activos para alimentos.
6. Análisis bibliométrico basado en Nanoencapsulación
Se realizó una búsqueda en la base de datos Scopus el 6 de mayo de 2023, utilizando como palabras clave “Nanoencapsulación”, “Compues-tos bioactivos” y “plantas medicinales”. Como resultado, se obtuvieron 141 documentos, los cuales fueron analizados posteriormente mediante los softwares VosViewer (versión 1.6.20) y Bibliometrix (Biblioshiny).
Con VosViewer se generó un mapa de coocurren-cias que permite visualizar las relaciones entre las palabras clave más relevantes en el campo (Figura 5a). En dicho mapa se identificó un clúster principal donde se agrupan los términos más importantes, además de que los colores reflejan la relación entre los años y la frecuencia de aparición de dichas palabras. Se observan los términos más comunes vinculados a la nanoencapsulación y sus agrupaciones temáticas, destacando conceptos como nanoencapsulation, particle size, drug delivery system, antioxidant, zeta potential y bioactive compounds, los cuales representan los núcleos principales en las áreas de investigación. Asimismo, los colores indican el año promedio de publicación asociado a cada término, permitiendo apreciar la evolución temática a lo largo del tiempo. Como ejemplo, términos como drug delivery system y zeta potential se relacionan con investigaciones más recientes, mientras que otros como encapsulation o plant extract predominan en estudios anteriores.
Por otra parte, con Bibliometrix se obtuvo una nube de palabras (wordcloud) (Figura 5b). En esta visualización, las palabras clave más frecuentes en el conjunto de datos aparecen en un esquema en forma de estrella, donde el tamaño de cada término indica la cantidad de veces que fue mencionado. La presencia destacada de términos como nanoencapsulation, particle size, bioactive compounds y chemistry subraya su relevancia en la literatura científica reciente. Esta representación facilita una comprensión rápida y visual de los temas predominantes en las investigaciones sobre nanoencapsulación a través del tiempo.
El dendrograma jerárquico (Figura 5c) organiza las palabras clave en torno a su similitud temática, confirmando y complementando las agrupaciones del MCA. Se identifican cinco clústeres principales: Clúster 1 (rojo): Bioactive compounds, actuando como un nodo central que conecta con diversos enfoques investigativos. Clúster 2 (azul): Técnicas de caracterización instrumental, destacando zeta potential, controlled study y Fourier transform infrared spectroscopy. Clúster 3 (verde): Propiedades funcionales y formulación, incluyendo chemistry, antioxidant, drug formulation y emulsion. Clúster 4 (morado): Técnicas de encapsulación, con los términos nanoencapsulation y encapsulation. Clúster 5 (naranja): Sistemas de liberación y fuentes naturales, agrupando particle size, unassigned drug, drug delivery system, plant extract y nanoparticle.
Estas agrupaciones reflejan la diversidad de enfoques en la investigación sobre nanoencap-sulación, desde técnicas y formulaciones hasta fuentes naturales y compuestos bioactivos emergentes.
En el mapa conceptual (Figura 5d), generado mediante análisis de correspondencias múltiples (MCA), se ilustran las principales dimensiones semánticas que organizan el campo investigativo. Se distinguen cinco agrupaciones temáticas. (a) Formulación y caracterización fisicoquímica: agrupa términos como zeta potential, controlled study y Fourier transform infrared spectroscopy, reflejando el enfoque técnico y analítico dominante en las etapas iniciales de investigación. (b) Compuestos naturales y bioactivos: Representado por palabras como antioxidant, chemistry, emulsion y drug formulation, lo que indica un interés creciente en utilizar materiales de origen natural en la nanoencapsulación. (c) Técnicas analíticas: Incluye términos como Fourier transform infrared spectroscopy y zeta potential, esenciales para la caracterización de los sistemas nanoestructurados. (Esta agrupación se superpone con el grupo anterior en el mapa, lo cual sugiere una conexión entre análisis instrumental y formulación).
(d) Extractos vegetales y sistemas de liberación: Se observa una agrupación centrada en plant extract, nanoparticle, drug delivery system, unassigned drug y particle size, lo que sugiere un enfoque en aplicaciones farmacéuticas y el uso de matrices vegetales como fuentes funcionales. (e) Encapsulación de compuestos funcionales: Ubicada en una zona intermedia del mapa, esta categoría incluye términos como nanoencapsulation y encapsulation, reflejando su rol como eje articulador de múltiples enfoques en el campo.
El posicionamiento de los términos en el mapa refleja su papel dentro del campo: los términos cercanos al centro representan temas trans-versales que articulan diferentes áreas, mientras que los términos periféricos corresponden a enfoques especializados o emergentes.
7. Conclusiones
La nanoencapsulación ha demostrado ser una herramienta eficaz para mejorar la estabilidad y biodisponibilidad de compuestos bioactivos extraídos de plantas medicinales infravaloradas, lo que facilita su incorporación en alimentos fun-cionales sin comprometer sus propiedades senso-riales y potencia sus beneficios terapéuticos.
Esta tecnología protege compuestos sensibles, como antioxidantes y principios activos de plantas medicinales, frente a condiciones adversas durante el procesamiento, almacenamiento y consumo, aumentando su efectividad biológica y abriendo nuevas posibilidades en aplicaciones nutracéuticas y farmacéuticas.
A pesar del avance tecnológico, persisten desafíos en cuanto a la escalabilidad, estabilidad a largo plazo y sostenibilidad de los sistemas de nanoencapsulación, aspectos que requieren mayor investigación para asegurar su viabilidad comercial e industrial.
El aprovechamiento de plantas medicinales tradicionales subutilizadas mediante nanoencap-sulación representa una estrategia prometedora para superar limitaciones de solubilidad y estabilidad, promoviendo un uso más eficiente y sostenible de recursos naturales ancestrales, en sintonía con los principios de la economía verde y la medicina natural.
Los análisis bibliométricos y técnicos indican que las áreas de mayor desarrollo incluyen formulación, caracterización, técnicas analíticas y el uso de materiales naturales, lo que facilita la transferencia de conocimiento científico a la industria y fomenta la innovación en la producción de alimentos funcionales y nutracéuticos.
Referencias bibliográficas
Abdul Khalil, H. P. S., Saurabh, C. K., Tye, Y. Y., Lai, T. K., Easa, A. M., Rosamah, E., Fazita, M. R. N., Syakir, M. I., Adnan, A. S., Fizree, H. M., Aprilia, N. A. S., & Banerjee, A. (2017). Seaweed based sustainable films and composites for food and pharmaceutical applications: A review. Renewable and Sustainable Energy Reviews, 77, 353-362. https://doi.org/10.1016/j.rser.2017.04.025
Abka-khajouei, R., Tounsi, L., Shahabi, N., Patel, A. K., Abdelkafi, S., & Michaud, P. (2022). Structures, Properties and Applications of Alginates. Marine Drugs, 20(6), 364. https://doi.org/10.3390/md20060364
Ahmed, J., Mulla, M., Jacob, H., Luciano, G., T.b., B., & Almusallam, A. (2019). Polylactide/poly(ε-caprolactone)/zinc oxide/clove essential oil composite antimicrobial films for scrambled egg packaging. Food Packaging and Shelf Life, 21, 100355. https://doi.org/10.1016/j.fpsl.2019.100355
Álvarez-Viñas, M., Souto, S., Flórez-Fernández, N., Torres, M. D., Bandín, I., & Domínguez, H. (2021). Antiviral Activity of Carrageenans and Processing Implications. Marine Drugs, 19(8), Article 8. https://doi.org/10.3390/md19080437
Arado, G. M., Amatto, P. D. P. G., Marins, M., Rizzi, E. S., França, S. D. C., Coppede, J. D. S., Carmona, F., & Pereira, A. M. S. (2024). Anti-inflammatory and/or immunomodulatory activities of Uncaria tomentosa (cat’s claw) extracts: A systematic review and meta-analysis of in vivo studies. Frontiers in Pharmacology, 15. https://doi.org/10.3389/fphar.2024.1378408
Assadpour, E., & Mahdi, S. (2019). A systematic review on nanoencapsulation of food bioactive ingredients and nutraceuticals by various nanocarriers. Critical Reviews in Food Science and Nutrition, 59(19), 3129-3151. https://doi.org/10.1080/10408398.2018.1484687
Bazana, M. T., Codevilla, C. F., & De Menezes, C. R. (2019). Nanoencapsulation of bioactive compounds: Challenges and perspectives. Current Opinion in Food Science, 26, 47-56. https://doi.org/10.1016/j.cofs.2019.03.005
Benitez, A. R., Margalit, D., Ryskin, M., Dor, M., Shuali, U., Nir, S., Polubesova, T., Ben-Ari, J., Kertsnus-Banchik, J., & Undabeytia, T. (2022). Modified Compositions of Micelle–Clay and Liposome–Clay Composites for Optimal Removal from Water of Bacteria and Hydrophobic Neutral Chemicals. Applied Sciences, 12(6), 3044. https://doi.org/10.3390/app12063044
Blanco-Llamero, C., Fonseca, J., Durazzo, A., Lucarini, M., Santini, A., Señoráns, F. J., & Souto, E. B. (2022). Nutraceuticals and Food-Grade Lipid Nanoparticles: From Natural Sources to a Circular Bioeconomy Approach. Foods, 11(15), Article 15. https://doi.org/10.3390/foods11152318
Bokov, D., Turki Jalil, A., Chupradit, S., Suksatan, W., Javed Ansari, M., Shewael, I. H., Valiev, G. H., & Kianfar, E. (2021). Nanomaterial by Sol-Gel Method: Synthesis and Application. Advances in Materials Science and Engineering, 2021(1), 5102014. https://doi.org/10.1155/2021/5102014
Boostani, S., & Jafari, S. M. (2021). A comprehensive review on the controlled release of encapsulated food ingredients; fundamental concepts to design and applications. Trends in Food Science & Technology, 109, 303-321. https://doi.org/10.1016/j.tifs.2021.01.040
Bušić, A., Komes, D., Vojvodić Cebin, A., Špoljarić, I., Mršić, G., & Miao, S. (2018). The Potential of Combined Emulsification and Spray Drying Techniques for Encapsulation of Polyphenols from Rosemary (Rosmarinus officinalis L.) Leaves. Food Technology and Biotechnology, 56(4). https://doi.org/10.17113/ftb.56.04.18.5680
Chandel, V., Biswas, D., Roy, S., Vaidya, D., Verma, A., & Gupta, A. (2022). Current Advancements in Pectin: Extraction, Properties and Multifunctional Applications. Foods, 11(17), Article 17. https://doi.org/10.3390/foods11172683
Dong, Y., Wei, Z., & Xue, C. (2021). Recent advances in carrageenan-based delivery systems for bioactive ingredients: A review. Trends in Food Science & Technology, 112, 348-361. https://doi.org/10.1016/j.tifs.2021.04.012
Delshadi, R., Bahrami, A., Tafti, A. G., Barba, F. J., & Williams, L. L. (2020). Micro and nano-encapsulation of vegetable and essential oils to develop functional food products with improved nutritional profiles. Trends in Food Science & Technology, 104, 72-83. https://doi.org/10.1016/j.tifs.2020.07.004
Hosseini, H., & Jafari, S. M. (2020). Introducing nano/microencapsulated bioactive ingredients for extending the shelf-life of food products. Advances in Colloid and Interface Science, 282, 102210. https://doi.org/10.1016/j.cis.2020.102210
Kamble, M. G., Singh, A., Singh, S. V., Kamble, M. G., Sagar, N. A., & Rani, N. (2025). Nanotechnology for encapsulation of bioactive components: A review. Discover Food, 5(1), 116. https://doi.org/10.1007/s44187-025-00386-7
Khajavian, M., Vatanpour, V., Castro-Muñoz, R., & Boczkaj, G. (2022). Chitin and derivative chitosan-based structures — Preparation strategies aided by deep eutectic solvents: A review. Carbohydrate Polymers, 275, 118702. https://doi.org/10.1016/j.carbpol.2021.118702
Kizilay, E., Kayitmazer, A. B., & Dubin, P. L. (2011). Complexation and coacervation of polyelectrolytes with oppositely charged colloids. Advances in Colloid and Interface Science, 167(1-2), 24-37. https://doi.org/10.1016/j.cis.2011.06.006
Linares-Otoya, V. (2020). Consideraciones para el uso y estudio de la “muña” peruana Minthostachys mollis (Benth.) Griseb y Minthostachys setosa (Briq.) Epling. Ethnobotany Research and Applications, 19. https://doi.org/10.32859/era.19.29.1-9
Liu, Z., Ye, L., Xi, J., Wang, J., & Feng, Z. (2021). Cyclodextrin polymers: Structure, synthesis, and use as drug carriers. Progress in Polymer Science, 118, 101408. https://doi.org/10.1016/j.progpolymsci.2021.101408
Najafian, Y., Hamedi, S. S., Farshchi, M. K., & Feyzabadi, Z. (2018). Plantago major in Traditional Persian Medicine and modern phytotherapy: A narrative review. Electronic Physician, 10(2), 6390-6399. https://doi.org/10.19082/6390
Norkaew, O., Thitisut, P., Mahatheeranont, S., Pawin, B., Sookwong, P., Yodpitak, S., & Lungkaphin, A. (2019). Effect of wall materials on some physicochemical properties and release characteristics of encapsulated black rice anthocyanin microcapsules. Food Chemistry, 294, 493-502. https://doi.org/10.1016/j.foodchem.2019.05.086
Park, H., Kim, J.-S., Kim, S., Ha, E.-S., Kim, M.-S., & Hwang, S.-J. (2021). Pharmaceutical Applications of Supercritical Fluid Extraction of Emulsions for Micro-/Nanoparticle Formation. Pharmaceutics, 13(11), 1928. https://doi.org/10.3390/pharmaceutics13111928
Pateiro, M., Gómez, B., Munekata, P. E. S., Barba, F. J., Putnik, P., Kovačević, D. B., & Lorenzo, J. M. (2021). Nanoencapsulation of Promising Bioactive Compounds to Improve Their Absorption, Stability, Functionality and the Appearance of the Final Food Products. Molecules, 26(6), 1547. https://doi.org/10.3390/molecules26061547
Peres, I. S. A., Conceição, K. A. O., Silva, L. A. F., Khouri, N. G., Yoshida, C. M. P., Concha, V. O. C., Lucarini, M., Durazzo, A., Santini, A., Souto, E. B., & Severino, P. (2023). Dragon’s Blood: Antioxidant properties for nutraceuticals and pharmaceuticals. Rendiconti Lincei. Scienze Fisiche e Naturali, 34(1), 131-142. https://doi.org/10.1007/s12210-022-01122-4
Ranakoti, L., Gangil, B., Mishra, S. K., Singh, T., Sharma, S., Ilyas, R. A., & El-Khatib, S. (2022). Critical Review on Polylactic Acid: Properties, Structure, Processing, Biocomposites, and Nanocomposites. Materials, 15(12), Article 12. https://doi.org/10.3390/ma15124312
Rohasmizah, H., & Azizah, M. (2022). Pectin-based edible coatings and nanoemulsion for the preservation of fruits and vegetables: A review. Applied Food Research, 2(2), 100221. https://doi.org/10.1016/j.afres.2022.100221
Sriwidodo, Umar, Abd. K., Wathoni, N., Zothantluanga, J. H., Das, S., & Luckanagul, J. A. (2022). Liposome-polymer complex for drug delivery system and vaccine stabilization. Heliyon, 8(2), e08934. https://doi.org/10.1016/j.heliyon.2022.e08934
Taher, M., Amri, M. S., Susanti, D., Abdul Kudos, M. B., Md Nor, N. F. A., & Syukri, Y. (2020). Medicinal Uses, Phytochemistry and Pharmacological Properties of Piper aduncum L. Sains Malaysiana, 49(8), 1829-1851. https://doi.org/10.17576/jsm-2020-4908-07
Tahir, A., Shabir Ahmad, R., Imran, M., Ahmad, M. H., Kamran Khan, M., Muhammad, N., Nisa, M. U., Tahir Nadeem, M., Yasmin, A., Tahir, H. S., Zulifqar, A., & Javed, M. (2021). Recent approaches for utilization of food components as nano-encapsulation: A review. International Journal of Food Properties, 24(1), 1074-1096. https://doi.org/10.1080/10942912.2021.1953067
Taouzinet, L., Djaoudene, O., Fatmi, S., Bouiche, C., Amrane-Abider, M., Bougherra, H., Rezgui, F., & Madani, K. (2023). Trends of Nanoencapsulation Strategy for Natural Compounds in the Food Industry. Processes, 11(5), Article 5. https://doi.org/10.3390/pr11051459
Tzounis, L., & Bangeas, P. (2022). Chapter 2—3D printing and nanotechnology. En V. N. Papadopoulos, V. Tsioukas, & J. S. Suri (Eds.), 3D Printing: Applications in Medicine and Surgery Volume 2 (pp. 7-26). Elsevier. https://doi.org/10.1016/B978-0-323-66193-5.00002-2
Zhang, K., Xu, Y., Lu, L., Shi, C., Huang, Y., Mao, Z., Duan, C., Ren, X., Guo, Y., & Huang, C. (2021). Hydrodynamic cavitation: A feasible approach to intensify the emulsion cross-linking process for chitosan nanoparticle synthesis. Ultrasonics Sonochemistry, 74, 105551. https://doi.org/10.1016/j.ultsonch.2021.105551
Umar, A. K., Wathoni, N., Zothantluanga, J. H., Das, S., & Luckanagul, J. A. (2022). Liposome-polymer complex for drug delivery system and vaccine stabilization. Heliyon, 8(2). https://doi.org/10.1016/j.heliyon.2022.e08934