Actividad fungistática y fungicida de compuestos bioactivos sobre el crecimiento in vitro de Moniliophthora roreri
Fungistatic and fungicidal activity of bioactive compounds on the in vitro growth of Moniliophthora roreri
Dario De la Cruz-Ricardez1*; Luz del Carmen Lagunes-Espinoza2*; Carlos Fredy Ortiz-García2; Ramón Marcos Soto-Hernández3; Edith Hernández-Nataren2
1 Tecnológico Nacional de México, Instituto Tecnológico de Huimanguillo. Carretera del Golfo Malpaso-El Bellote km. 98.5, Col. Ranchería Libertad. 86400 Huimanguillo, Tabasco, México.
2 Posgrado en Ciencias Agrícolas en el Trópico. Colegio de Postgraduados-Tabasco. 86500 H. Cárdenas, Tabasco, México.
3 Posgrado en Botánica. Colegio de Postgraduados-Montecillo. 56264 Montecillo, Texcoco, Edo. de México, México.
ORCID de los autores
D. De la Cruz-Ricardez: https://orcid.org/0000-0002-5171-4797 L. C. Lagunes-Espinoza: https://orcid.org/0000-0002-1632-5278
C. F. Ortiz-García: https://orcid.org/0000-0002-6820-9252 R. M. Soto-Hernández: https://orcid.org/0000-0001-8577-7991
E. Hernández-Nataren: https://orcid.org/0000-0003-2109-2111
RESUMEN
La moniliasis del cacao, causada por Moniliophthora roreri, es una de las principales limitantes en la producción de cacao en Latinoamérica. El control basado en prácticas culturales y fungicidas sintéticos puede resultar costoso y con riesgos ambientales y para la salud. Este estudio evaluó in vitro la actividad antifúngica de los compuestos bioactivos (CB), ácido benzoico (ABE), ácido gálico (AGA), catequina (CAT), quercetina (QUE) y β-caroteno (BCA), además de una mezcla (MIX) entre ellos. Se evaluaron tres concentraciones (500, 1000 y 2000 mg L⁻¹) sobre el crecimiento micelial de M. roreri. Se realizó un ANDEVA con prueba de Tukey (α = 0,05) y un análisis de componentes principales (ACP). Los resultados mostraron que el ABE fue más eficiente, con efecto fungicida a partir de 1000 mg L⁻¹ y un IC₅₀ < 500 mg L⁻¹. El BCA y el AGA presentaron efectos fungistáticos dosis-dependientes. La CAT evidenció un comportamiento hormético, mientras que la MIX no mostró efectos sinérgicos. El ABE y BCA destacan como candidatos prometedores para el desarrollo de biofungicidas contra M. roreri.
Palabras clave: Moniliasis del cacao; Metabolitos secundarios; ácidos fenólicos; flavonoides; β-caroteno.
ABSTRACT
Frosty pod rot, caused by Moniliophthora roreri, is one of the main constraints on cacao production in Latin America. Control strategies based on cultural practices and synthetic fungicides can be costly and pose environmental and health risks. This study evaluated in vitro the antifungal activity of the bioactive compounds (BCs) benzoic acid (BA), gallic acid (GA), catechin (CAT), quercetin (QUE), and β-carotene (BCA), as well as a mixture (MIX) of these compounds. Three concentrations (500, 1000, and 2000 mg L⁻¹) were tested on the mycelial growth of M. roreri. Data were analyzed using analysis of variance (ANOVA) followed by Tukey’s test (α = 0.05) and principal component analysis (PCA). The results showed that BA was the most effective compound, exhibiting a fungicidal effect at concentrations ≥1000 mg L⁻¹ and an IC₅₀ < 500 mg L⁻¹. BCA and GA showed dose-dependent fungistatic effects. CAT exhibited a hormetic response, whereas the MIX showed no synergistic effects. BA and BCA stand out as promising candidates for the development of biofungicides against M. roreri.
Keywords: Cacao frosty pod rot; secondary metabolites; phenolic acids; flavonoids; β-carotene.
1. Introducción
Tradicionalmente, el control de las enfermedades fúngicas en los cultivos frutícolas se ha basado en prácticas culturales, complementadas en algunos casos con fungicidas sintéticos. Si bien estas medidas pueden reducir la incidencia de las enfermedades, aún presentan limitaciones importantes. En el cultivo de cacao, una de las principales enfermedades en Latinoamérica es la moniliasis, ocasionada por M. roreri (Cif. y Par.) Evans et al., (Bailey et al., 2018). Su manejo se basa en la poda, manejo de la sombra, eliminación de frutos enfermos y aplicaciones de fungicidas (Ortiz-García et al., 2015; Torres-De la Cruz et al., 2019). Sin embargo, tener un manejo eficiente de la enfermedad implica costos elevados, riesgos de contaminación ambiental y para la salud humana, además del riesgo de expansión por países donde no hay presencia (Plasencia-Vázquez et al., 2022). Ante este escenario, es necesario explorar alternativas de manejo más sostenibles, amigables con la salud humana y el ambiente.
En la última década, los metabolitos secundarios o CB de origen vegetal han adquirido relevancia como posibles agentes de control de hongos fitopatógenos (Deresa y Diriba, 2023). En el caso de M. roreri se han reportado múltiples trabajos con extractos de plantas con muy buenos resultados (Tamayo España et al., 2017; De la Cruz-Ricardez et al., 2020; Fuentes-Estrada et al., 2023). Estos compuestos activos presentes en los extractos vegetales son parte de los mecanismos de defensa de las plantas, incluyen diversas familias químicas, pero se caracterizan en cinco principales, terpenoides (terpenos volátiles, esteroides y carotenoides), fenólicos (flavonoides, cumarina y taninos), nitrogenados (alcaloides, glucósidos cianogénicos, aminoácidos no proteicos, amidas de ácidos grasos), azufrados (glucosinolatos, tiosulfinatos y lectinas) y otros compuestos como cicloparafinas, alquenos, alquinos y compuestos halogenados (Al-Khayri et al., 2023). La actividad antifúngica de los CB puede manifestarse a través de múltiples mecanismos como la alteración de la permeabilidad de la membrana celular, inhibición de enzimas clave en el metabolismo del hongo, interferencia en la síntesis de la pared celular o generación de estrés oxidativo (Yang et al., 2024). Además, al provenir de fuentes naturales, suelen ser más biodegradables y menos tóxicos para organismos no objetivo, lo que favorece su incorporación a estrategias de manejo integrado de enfermedades.
En particular, los ácidos fenólicos, han sido reportados como potentes inhibidores del crecimiento micelial en diversas especies fúngicas, gracias a su capacidad para desestabilizar estructuras celulares y afectar procesos bioquímicos esenciales (Xu et al., 2018; Joaquín-Ramos et al., 2020; Xu et al., 2022). Los flavonoides, poseen propiedades antioxidantes y antimicrobianas, aunque su eficacia antifúngica depende de factores como la dosis, el pH y la interacción con otros metabolitos (McNally et al., 2003; Del Río et al., 2004; Dias et al., 2021; Ramaroson et al., 2022; Lee et al., 2024; Castano-Duque et al., 2024). Por su parte, los carotenoides, además de su función antioxidante, pueden modular la respuesta oxidativa de los patógenos y afectar su desarrollo (Rodriguez-Maturino et al., 2015; Askari et al., 2023).
La evaluación comparativa de la actividad fungistática y fungicida de estos metabolitos frente a M. roreri permitirá identificar compuestos con potencial para su implementación en el manejo de la moniliasis del cacao. Asimismo, el análisis de su eficacia en función de la concentración y del tipo de compuesto puede aportar información valiosa sobre sus mecanismos de acción y posibles sinergias (Freiesleben et al., 2014).
En este contexto, se planteó este trabajo con el objetivo de evaluar el efecto inhibitorio de ácidos fenólicos (AGA y ABE), flavonoides (CAT y QUE) y un carotenoide (BCA) sobre el crecimiento micelial de M. roreri.
2. Metodología
2.1 Obtención de reactivos
Los reactivos estándares de AGA, ABE, QUE, CAT, BCA se adquirieron de Sigma-Aldrich, Inc. (St. Louis, MO, EE. UU.). Para el medio de cultivo se utilizó Agar y carbonato de calcio, adquiridos de Mercalab.
2.2 Obtención de M. roreri
El aislamiento de M. roreri (CPMR21-04) fue proporcionado por el Laboratorio de Fitopatología del Colegio de Postgraduados, Campus Tabasco, previamente fue identificado morfológicamente de acuerdo a la forma, coloración y crecimiento de las colonias, además de forma de las esporas (Evans, 1981) y se preservó en colonias desa-rrolladas en medio de cultivo V8 hasta su uso.
2.3 Preparación de tratamientos
A partir de compuestos bioactivos estándares (CB) se prepararon tres concentraciones (500, 1000 y 2000 mg L⁻¹). Para ello, se elaboró una solución madre de 2500 mg L⁻¹, de la cual se realizaron diluciones sucesivas con agua destilada. El tiempo necesario para lograr la disolución completa varió según el compuesto, dependiendo de su solubilidad, por lo que fue necesario proteger las soluciones de la luz durante su preparación.
Se elaboró 1 L de medio de cultivo V8 clarificado, que posteriormente fue esterilizado en autoclave a 121 °C durante 15 min. Luego de la esterilización, y antes de que el medio solidificara, se añadió el volumen correspondiente de cada solución diluida de los compuestos estándares, utilizando jeringas con filtros Acrodisc® de 0,20 µm (Corning®, Alemania), para mantener la asepsia del medio. Las mezclas fueron homoge-neizadas en una plancha de calentamiento.
Posteriormente, se vertieron 5 mL del medio suplementado en cajas de Petri de 60 mm de diámetro. Una vez solidificado, se sembraron discos de micelio (15 días de crecimiento) del aislamiento CPMR21-04 de M. roreri. Cada caja de Petri fue considerada una unidad experimental, y se establecieron 10 repeticiones por tratamiento. Las cajas fueron incubadas a 25 °C en oscuridad, durante todo el experimento.
2.4 Inhibición del crecimiento micelial
El crecimiento micelial de las colonias de M. roreri se midió con un vernier en mm, tomando dos lecturas en ejes ortogonales (perpendiculares) para cada caja de Petri. Las mediciones se realizaron cada 24 h en condiciones de luz baja. Las medidas se dieron por concluidas cuando las colonias del tratamiento testigo cubrieron completamente la superficie del medio de cultivo. A partir de ese momento, se calculó la eficiencia de inhibición del crecimiento micelial.
2.5 Eficiencia de inhibición del crecimiento micelial
Con los datos de inhibición del crecimiento micelial obtenidos, se calculó la eficiencia de los tratamientos con compuestos en comparación con el testigo mediante la ecuación 1:
E = [(Vt − Vce) / Vt] × 100 (1)
Donde: E es la eficiencia de inhibición (%); Vt es el valor promedio del crecimiento en el testigo y Vce el valor promedio del crecimiento en el tratamiento con el compuesto estándar.
2.6 Determinación de la concentración media inhibitoria (IC₅₀)
A partir de los valores de E (%) obtenidos para cada concentración (500, 1000 y 2000 mg L⁻¹), se determinó la concentración media inhibitoria (IC₅₀), definida como la dosis necesaria para inhibir el 50% del crecimiento micelial. Para cada dosis, se calculó el promedio de las réplicas experimentales y se identificó el intervalo de concentraciones cuyas eficiencias promedio flan-quearon el 50%. La IC₅₀ se estimó por inter-polación lineal en escala logarítmica, mediante la ecuación 2 (Motulsky & Christopoulos, 2003):
log10(IC50) = log10(Ca) + [(50 – Ia) / (Ib – Ia)] × [log10(Cb) − log10(Ca)] (2)
Donde Ca: concentración inmediatamente inferior a aquella en la que se alcanza el 50% de inhibición del crecimiento micelial; Cb: concentración inmediatamente superior a aquella en la que se alcanza el 50% de inhibición del crecimiento micelial; Ia: eficiencia promedio de inhibición (%) observada a la concentración Ca; Ib: eficiencia promedio de inhibición (%) observada a la concentración Cb.
El valor final de IC₅₀ se obtuvo transformando nuevamente a escala lineal mediante la ecuación:
IC50 = 10log10(IC50) (3)
Cuando todas las concentraciones evaluadas presentaron inhibiciones ≥ 50%, la IC₅₀ se reportó como menor que la concentración mínima eva-luada; mientras que, si todas las concentraciones presentaron inhibiciones ≤ 50%, se reportó como no calculada.
2.7 Diseño experimental y análisis de datos
Se empleó un diseño completamente al azar, considerando como tratamientos cada compuesto estándar con sus respectivas concentraciones (18 en total) más un testigo, con 10 repeticiones por tratamiento. Los datos de eficiencia, expresados en porcentaje, fueron transformados mediante la función arcoseno de la raíz cuadrada para estabilizar la varianza y aproximar la distribución a la normalidad. Se aplicó un análisis de varianza (ANDEVA) para detectar diferencias significativas entre tratamientos, seguido de la prueba de Tukey (α = 0,05) cuando se identificaron diferencias estadísticas (p < 0,05), utilizando InfoStat, v. 2020. Adicionalmente, se realizó un análisis de componentes principales (ACP) para explorar la relación entre los metabolitos secundarios y su eficiencia de inhibición sobre M. roreri. Para ello, se empleó el software R versión 4.2.2.
3. Resultados y discusión
3.1 Inhibición del crecimiento micelial
El efecto de los CB estándares sobre el crecimiento micelial de M. roreri en condiciones in vitro fue muy variable (Figura 1). En general, la mayoría de los compuestos evaluados mostraron una inhibición progresiva del desarrollo del hongo a medida que aumentó la concentración. El ABE fue el tratamiento más eficaz, ya que este logró una inhibición completa del crecimiento micelial a partir de 1000 mg L⁻¹, seguido del AGA, que también mostró una reducción significativa del micelio. En contraste, la CAT presentó un comportamiento inverso, ya que se observó un incremento en el crecimiento micelial de M. roreri con el aumento de la concentración, lo que sugiere un posible efecto estimulante para su crecimiento.
Este comportamiento diferencial puede explicarse por la naturaleza y función biológica de los CB. Estas moléculas generadas a partir de metabolitos primarios mediante vías metabólicas secundarias, no son necesarios para el crecimiento y la reproducción de las plantas; sin embargo, cada vez hay más evidencia que demuestra que los CB contribuyen significativamente a la defensa contra microorganismos patógenos especialmente hongos (Sukrasno, 2018; Wang et al., 2024). La actividad antifúngica de los CB depende de su estructura química, concentración y del patógeno objetivo, lo que explica la variabilidad observada entre tratamientos.
En concordancia con los resultados del presente estudio, De la Cruz-Ricardez et al. (2020) reportaron que el extracto de compuestos fenólicos de frutos inmaduros de C. annuum var. glabriusculum inhibe en un 95% de inhibición micelial de M. roreri a 2500 mg L⁻¹ y suprime totalmente su esporulación lo que correspondería a un efecto fungicida para sus células reproductoras. Asimismo, Rodríguez-Maturino et al. (2015), reportaron efectos fungistáticos de extractos fenólicos y de carotenoides de frutos de la misma especie sobre el crecimiento micelial y la germinación de conidios de Alternaria alternata y Fusarium oxysporum. Sin embargo, no hay reportes del efecto de compuestos puros sobre M. roreri. Por lo que, hasta donde tenemos conocimiento, este estudio constituye el primer reporte de la actividad antifúngica de los compuestos puros sobre M. roreri.
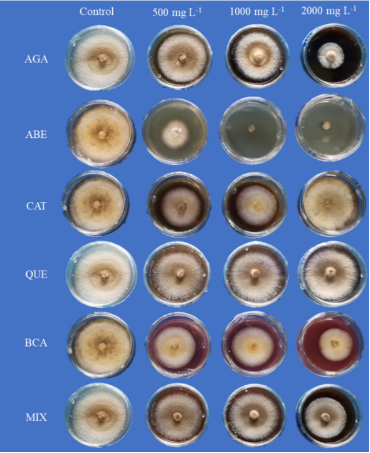
Figura 1. Crecimiento micelial in vitro de Moniliophthora roreri en presencia de compuestos estándares a concentraciones de 500, 1000 y 2000 mg L-1. AGA, Ácido gálico; ABE, Ácido benzoico; CAT, Catequina; QUE, Quercetina; BCA, β-caroteno; MIX, Mezcla de compuestos.
Figure 1. In vitro mycelial growth of Moniliophthora roreri in the presence of standard compounds at concentrations of 500, 1000 and 2000 mg L-1. AGA, Gallic acid; ABE, Benzoic acid; CAT, Catechin; QUE, Quercetin; BCA, β-carotene; MIX, Mixture of compounds.
3.2 Eficiencia de inhibición del crecimiento micelial
La eficiencia de inhibición (%) del crecimiento micelial de M. roreri varió en función del CB y la concentración del mismo. En términos generales, se observó una respuesta diferencial entre los grupos químicos evaluados, lo que evidencia que la actividad antifúngica depende tanto de la naturaleza del metabolito como de la dosis aplicada. Entre los ácidos fenólicos evaluados, el ABE fue el más eficaz, que mostró una eficiencia superior al 80% desde la concentración más baja (500 mg L⁻¹) y logrando una inhibición completa del crecimiento micelial a 1000 y 2000 mg L⁻¹, concentraciones que no presentaron diferencias estadísticas significativas entre sí (Figura 2). Este comportamiento indica un efecto inhibitorio fuerte y consistente. Por su parte, el AGA evidenció una clara respuesta dosis-dependiente, que mostró una eficiencia de inhibición superior al 90% a la mayor concentración evaluada (2000 mg L⁻¹).
Un patrón similar de respuesta dosis-dependiente se observó en el carotenoide BCA, aunque con una eficacia menor en comparación con los ácidos fenólicos. El BCA mostró eficiencias superiores al 60% desde 500 mg L⁻¹ y alcanzó una inhibición elevada (85%) a 2000 mg L⁻¹, lo que sugiere un efecto antifúngico moderado pero consistente.
En contraste, los flavonoides evaluados mostraron un comportamiento marcadamente distinto. La QUE presentó eficiencias de inhibición muy bajas (<20%) en todas las concentraciones evaluadas, sin diferencias significativas entre tratamientos. Por su parte, la CAT alcanzó una eficacia moderada por encima del 50% con las concentraciones de 500 y 1000 mg L⁻¹; sin embargo, con la concentración más alta (2000 mg L⁻¹) la eficiencia fue menor a 5%, lo que sugiere una pérdida de actividad antifúngica, o incluso que con altas concentraciones de CAT se estaría estimulando el crecimiento micelial del M. roreri bajo las condiciones evaluadas.
La marcada eficacia del ABE, con efecto fungicida a partir de 1000 mg L⁻¹ y manteniendo un efecto fungistático con 500 mg L⁻¹, concuerda con estudios previos que reportan la capacidad del ABE para alterar el gradiente de protones y la integridad de la membrana plasmática en hongos, lo que conduce a la pérdida de viabilidad celular (Berne et al., 2015). De manera similar, el efecto inhibitorio dosis-dependiente observado para el AGA ha sido atribuido a su capacidad para inducir estrés oxidativo y dañar macromoléculas celulares, afectando procesos vitales del hongo (Alves et al., 2013; Palacios et al., 2011).
Entre los flavonoides evaluados, la QUE mostró eficiencias muy bajas (<20%), lo que concuerda con reportes que indican que su actividad antifúngica suele ser limitada frente a basidiomicetos, posiblemente debido a su baja biodisponibilidad y solubilidad en medios acuosos (Cushnie y Lamb, 2011). Por el contrario, la CAT presentó un patrón atípico, inhibición moderada a 500 y 1000 mg L⁻¹, pero una drástica disminución de la actividad a 2000 mg L⁻¹, incluso se podría pensar en la estimulación del crecimiento micelial. Este comportamiento podría explicarse por un fenómeno de hormesis, un fenómeno de relación dosis-respuesta caracterizado por la estimulación con dosis bajas y la inhibición con dosis altas (Calabrese & Baldwin, 2003). Por lo que es necesario evaluar este efecto en futuros trabajos.
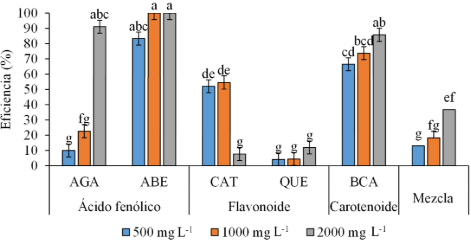
Figura 2. Eficiencia en la inhibición (%) del crecimiento de Moniliophthora roreri por ácidos fenólicos, flavonoides, carotenoide y mezcla de metabolitos a concentraciones de 500, 1000 y 2000 mg L⁻¹. Letras diferentes en las barras, indican diferencias significativas Tukey (α = 0,05).
Figure 2. Efficiency in the inhibition (%) of the growth of Moniliophthora roreri by phenolic acids, flavonoids, carotenoid and mixture of metabolites at concentrations of 500, 1000 and 2000 mg L⁻¹. Different letters on the bars indicate significant differences Tukey (α = 0.05).
En el caso del BCA, se observó una inhibición significativa, aunque inferior a la de los ácidos fenólicos, lo que sugiere un posible mecanismo indirecto de acción, probablemente asociado a la modulación de membranas o a su función antioxidante, tal como se ha descrito en carotenoides con actividad antimicrobiana moderada (Swapnil, 2021; Meléndez-Martínez et al., 2021; Abdulhafedh et al., 2023).
Finalmente, la MIX presentó un incremento en la eficiencia de inhibición conforme aumentó la concentración; sin embargo, no logró una inhibición completa del crecimiento micelial, ni siquiera a la concentración más alta evaluada (2000 mg L⁻¹), a diferencia del ABE aplicado de manera individual. Este comportamiento sugiere la ausencia de efectos sinérgicos y la posible presencia de interacciones antagónicas entre los compuestos, lo que limita su eficacia antifúngica cuando se aplican en conjunto. En consecuencia, la MIX no superó la actividad de los metabolitos más efectivos evaluados de forma individual, lo cual concuerda con lo reportado para combinaciones de compuestos fenólicos y otros metabolitos secundarios (Daglia, 2012; Wang et al., 2024).
3.3 Determinación de la concentración media inhibitoria (IC₅₀)
Los valores calculados de IC₅₀ de cada com-puesto mediante interpolación logarítmica entre las dos concentraciones adyacentes que enmar-can el 50% de inhibición, se muestran en el cuadro 1. El ABE y el BCA mostraron inhibiciones superiores al 50% incluso a la dosis más baja, por lo que sus IC₅₀ fueron < 500 mg L-1. El AGA alcanzó un valor próximo al 50% con 1000 mg L-1, por lo que obtuvo un IC50 de eficiencia con 1320 mg L-1. Similarmente se comportó la CAT que alcanzó un valor IC50 con 1070 mg L-1, en este caso a partir de esta concentración la eficiencia tiende a disminuir. Por su parte la QUE, y la mezcla no superaron el 50% de inhibición con las concentraciones evaluadas, resultando en IC₅₀ > 2000 mg L-1.
En la Tabla 1 se presentan los valores de concentración inhibitoria media (IC₅₀) obtenidos para cada compuesto. ABE y el BCA exhibieron porcentajes de inhibición superiores al 50% incluso en la menor concentración evaluada (500 mg L⁻¹), por lo que sus IC₅₀ se estimaron por debajo de dicho valor. El AGA alcanzó un nivel de inhibición cercano al 50% con 1000 mg L⁻¹, obteniéndose un IC₅₀ de 1320 mg L⁻¹. La catequina (CAT) mostró un comportamiento similar, con un IC₅₀ de 1070 mg L⁻¹, aunque su eficiencia presentó una tendencia decreciente a concentraciones superiores. Por el contrario, la quercetina (QUE) y la mezcla evaluada no lograron superar el 50% de inhibición en el intervalo de concentraciones ensayado, resultando en IC₅₀ superiores a 2000 mg L⁻¹.
Los valores de IC₅₀ inferiores a 500 mg L⁻¹ para el ABE y el BCA indican que estos CB poseen un alto potencial antifúngico contra Moniliophthora roreri. La elevada eficacia del ABE se asocia con su capacidad para alterar la integridad de la membrana plasmática y el metabolismo celular fúngico, mientras que el efecto fungistático del BCA podría relacionarse con la modulación del balance redox y la interacción con membranas celulares (Alves et al., 2013; Berne et al., 2015; Swapnil et al., 2021). No obstante, la validación de estos resultados requiere estudios in vivo y evaluaciones de fitotoxicidad, así como un análisis detallado de las interacciones entre metabolitos, dado que la ausencia de sinergia observada en la mezcla sugiere posibles efectos antagónicos que pueden limitar su aplicación como biofungicidas (Daglia, 2012; Freiesleben & Jäger, 2014) e integrarlos en el manejo sustentable de la moniliasis del cacao.
Tabla 1
Concentración inhibitoria media (IC₅₀) estimada para CB en la inhibición de Moniliophthora roreri
Compuesto estándar | IC50 estimada (mg L-1) |
Catequina (CAT) Quercetina (QUE) Ácido benzoico (ABE) Ácido gálico (AGA) β-caroteno (BCA) Mix (MIX) | 1070 NC < 500 1320 < 500 NC |
IC₅₀ estimada mediante interpolación logarítmica. NC= No calculada porque las eficiencias fueron bajas (< 50%).
3.4 Relación entre compuestos bioactivos y su eficiencia de inhibición sobre M. roreri
El ACP (Figura 3) muestra que cada grupo de metabolitos presenta un patrón independiente en cuanto a la magnitud de su efecto antifúngico, lo que podría estar asociado a diferencias en los mecanismos de acción entre los distintos tipos de compuestos. Los ácidos fenólicos muestran una mayor dispersión a lo largo del eje horizontal (PC1), lo que indica que no todos poseen el mismo nivel de eficacia frente al hongo. Por su parte, los flavonoides exhiben un patrón de inhibición claramente distinto al de los ácidos fenólicos, probablemente debido a variaciones en su estructura química, y en este caso mostraron una eficiencia diferente en la inhibición de M. roreri. El BCA, en cambio, presentó una menor variabilidad, manifestando un efecto inhibidor intermedio.
La efectividad antifúngica de cada CB sobre M. roreri en este trabajó dependió de la concentración aplicada y principalmente al grupo al que pertenece, el efecto de ácidos fenólicos, flavonoides y el carotenoide evaluado, puede ser el reflejo de las diferencias en polaridad, estructura química o en cómo afectan el metabolismo del hongo (Al-Khayri et al., 2023; Yang et al., 2024).
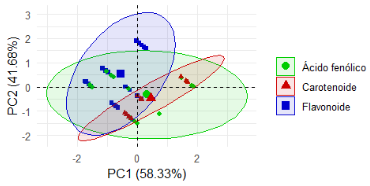
Figura 3. Análisis de componentes principales (ACP) de ácidos fenólicos, flavonoides y carotenoides, metabolitos según su tipo químico y según su patrón de efecto antifúngico.
Figure 3. Principal component analysis (PCA) of phenolic acids, flavonoids and carotenoids, metabolites according to their chemical type and according to their antifungal effect pattern.
4. Conclusiones
La eficiencia antifúngica de los compuestos están-dar frente a M. roreri es altamente dependiente del tipo de metabolito y de la concentración aplicada. El ácido benzoico destacó como un potente inhibidor del crecimiento micelial de M. roreri, logrando un efecto fungicida a concentraciones relativamente bajas (< 1000 mg L⁻¹). El β-caroteno y el ácido gálico también mostraron un efecto fungistático, aunque con respuestas dosis-dependientes más marcadas. Los flavonoides catequina y la quercetina presentaron una baja o nula eficacia a concentraciones elevadas, e incluso la catequina evidenció un posible efecto estimulante del crecimiento a altas dosis. La ausencia de sinergia en la mezcla de compuestos sugiere que las interacciones entre metabolitos pueden limitar su efectividad. Estos hallazgos aportan información valiosa para la selección de compuestos bioactivos presentes en plantas que tienen potencial para el control de M. roreri.
Contribución de los autores
D. De la Cruz-Ricardez: Curación de datos, análisis formal, software y redacción del borrador original. L. C. Lagunes-Espinoza: Conceptualización, metodología, administración del proyecto, revisión y edición de la redacción. C. F. Ortiz-García: Investigación, metodología y supervisión. E. Hernández-Nataren: Visualización y revisión. R. M. Soto-Hernández: Revisión y edición de la redacción. Todos los autores han leído y aceptado la versión publicada del manuscrito.
Consideraciones éticas
Este estudio no involucró experimentación con humanos ni animales.
Referencias bibliográficas
Abdulhafedh, H. M., Al-Saadoon, A. H., & Abu-Mejdad, N. M. (2023). Efficiency of fungal β-carotene against some causative agents of dermatomycoses. Iranian Journal of War and Public Health, 15(2), 167–175. https://doi.org/10.58209/ijwph.15.2.167
Al-Khayri, J. M., Rashmi, R., Toppo, V., Chole, P. B., Banadka, A., Sudheer, W. N., Nagella, P., Shehata, W. F., Al-Mssallem, M. Q., Alessa, F. M., Almaghasla, M. I., & Rezk, A. A.-S. (2023). Plant Secondary Metabolites: The Weapons for Biotic Stress Management. Metabolites, 13(6), 716. https://doi.org/10.3390/metabo13060716
Alves, M. J., Ferreira, I. C. F. R., Froufe, H. J. C., Abreu, R. M. V., Martins, A., & Pintado, M. (2013). Antimicrobial activity of phenolic compounds identified in wild mushrooms, SAR analysis and docking studies. Journal of Applied Microbiology, 115(2), 346–357. https://doi.org/10.1111/jam.12196
Bailey, B. A., Evans, H. C., Phillips-Mora, W., Ali, S. S., & Meinhardt, L. W. (2018). Moniliophthora roreri, causal agent of cacao frosty pod rot. Molecular Plant Pathology, 19(7), 1580–1594. https://doi.org/10.1111/mpp.12648
Berne, S., Kovačič, L., Sova, M., Kraševec, N., Gobec, S., Križaj, I., & Komel, R. (2015). Benzoic acid derivatives with improved antifungal activity: Design, synthesis, structure–activity relationship (SAR) and CYP53 docking studies. Bioorganic & Medicinal Chemistry, 23(15), 4264–4276. https://doi.org/10.1016/j.bmc.2015.06.042
Castano-Duque, L., Lebar, M. D., Mack, B. M., Lohmar, J. M., & Carter-Wientjes, C. (2024). Investigating the Impact of Flavonoids on Aspergillus flavus: Insights into Cell Wall Damage and Biofilms. Journal of Fungi, 10(9), 665. https://doi.org/10.3390/jof10090665
De la Cruz-Ricardez, D., Ortiz-García, C. F., Lagunes-Espinoza, L. C., & Torres-De la Cruz, M. (2020). Efecto antifúngico in vitro de extractos metanólicos de Capsicum spp. en Moniliophthora roreri. Agrociencia, 54, 813–824.
Del Río, J. A., Gómez, P., Baidez, A. G., Arcas, M. C., Botía, J. M., & Ortuño, A. (2004). Changes in the levels of polymethoxyflavones and flavanones as part of the defense mechanism of Citrus sinensis (cv. Valencia Late) fruits against Phytophthora citrophthora. Journal of Agricultural and Food Chemistry, 52(7), 1913–1917. https://doi.org/10.1021/jf030723i
Evans, H. C. (1981). Pod rot of cacao caused by Moniliophthora (Monilia) roreri. Phytopathological Papers, 24, 1–44.
Freiesleben, S. H., & Jäger, A. K. (2014). Correlation between plant secondary metabolites and their antifungal mechanisms – A review. Medicinal & Aromatic Plants, 3(2). https://doi.org/10.4172/2167-0412.1000154
Fuentes-Estrada, M., Jiménez-González, A., Duarte, D., Saavedra-Barrera, R., Areche, C., Stashenko, E., Pino Benítez, N., Bárcenas-Pérez, D., Cheel, J., & García-Beltrán, O. (2023). GC/MS Profile and Antifungal Activity of Zanthoxylum caribaeum Lam Essential Oil against Moniliophthora roreri Cif and Par, a Pathogen That Infects Theobroma cacao L Crops in the Tropics. Chemosensors, 11(8), 447. https://doi.org/10.3390/chemosensors11080447
Joaquín-Ramos, A. de J., López-Palestina, C. U., Pinedo-Espinoza, J. M., Altamirano-Romo, S. E., Santiago-Saenz, Y. O., Aguirre-Mancilla, C. L., & Gutiérrez-Tlahque, J. (2020). Phenolic compounds, antioxidant properties and antifungal activity of jarilla (Barkleyanthus salicifolius [Kunth] H. Rob & Brettell). Chilean Journal of Agricultural Research, 80(3), 352-360. https://dx.doi.org/10.4067/S0718-58392020000300352
Lee, J.-H., Kim, Y.-G., Park, I., & Lee, J. (2024). Antifungal and antibiofilm activities of flavonoids against Candida albicans: Focus on 3,2′-dihydroxyflavone as a potential therapeutic agent. Biofilm, 8, 100218. https://doi.org/10.1016/j.bioflm.2024.100218
McNally, D. J., Wurms, K. V., Labbé, C., & Bélanger, R. R. (2003). Synthesis of C-glycosyl flavonoid phytoalexins as a site-specific response to fungal penetration in cucumber. Physiological and Molecular Plant Pathology, 63(6), 293–303. https://doi.org/10.1016/j.pmpp.2004.03.005
Meléndez-Martínez, A. J., Mandić, A. I., Bantis, F., Böhm, V., Borge, G. I. A., Brnčić, M., & others. (2022). A comprehensive review on carotenoids in foods and feeds: Status quo, applications, patents, and research needs. Critical Reviews in Food Science and Nutrition, 62(8), 1999–2049. https://doi.org/10.1080/10408398.2020.1867959
Motulsky, H. J., & Christopoulos, A. (2003). Fitting models to biological data using linear and nonlinear regression: A practical guide to curve fitting. GraphPad Software, Inc.
Ortiz-García, C. F., Torres-De la Cruz, M., & Hernández-Mateo, S. C. (2015). Comparación de dos sistemas de manejo del cultivo del cacao, en presencia de Moniliophthora roreri, en México. Revista Fitotécnica Mexicana, 38, 191–196.
Palacios, I., Lozano, M., Moro, C., D’Arrigo, M., Rostagno, M. A., Martínez, J. A., García-Lafuente, A., Guillamón, E., & Villares, A. (2011). Antioxidant properties of phenolic compounds occurring in edible mushrooms. Food Chemistry, 128(3), 674–678. https://doi.org/10.1016/j.foodchem.2011.03.085
Plasencia-Vázquez, Alexis Herminio, Vilchez-Ponce, Cruz Ruby, Ferrer-Sánchez, Yarelys, & Veloz-Portillo, Carmen Elena. (2022). Efecto del cambio climático sobre la distribución potencial del hongo Moniliophthora roreri y el cultivo de cacao (Theobroma cacao) en Ecuador continental. Terra Latinoamericana, 40, e1151. https://doi.org/10.28940/terra.v40i0.1151
Ramaroson, M.-L., Koutouan, C., Helesbeux, J.-J., Le Clerc, V., Hamama, L., Geoffriau, E., & Briard, M. (2022). Role of Phenylpropanoids and Flavonoids in Plant Resistance to Pests and Diseases. Molecules, 27(23), 8371. https://doi.org/10.3390/molecules27238371
Rodriguez-Maturino, A., Troncoso-Rojas, R., Sánchez-Estrada, A., González-Mendoza, D., Ruiz-Sanchez, E., Zamora-Bustillos, R., Ceceña-Duran, C., Grimaldo-Juarez, O., & Aviles-Marin, M. (2015). Antifungal effect of phenolic and carotenoids extracts from chiltepin (Capsicum annum var. glabriusculum) on Alternaria alternata and Fusarium oxysporum. Revista Argentina de Microbiología, 47(1), 72–77. https://doi.org/10.1016/j.ram.2014.12.005
Swapnil, P., Meena, M., Singh, S. K., Dhuldhaj, U. P., Harish, & Marwal, A. (2021). Vital roles of carotenoids in plants and humans to deteriorate stress with its structure, biosynthesis, metabolic engineering and functional aspects. Current Plant Biology, 26, 100203. https://doi.org/10.1016/j.cpb.2021.100203
Tamayo España, L. E., Ramírez González, S. I., López Báez, O., Quiroga Madrigal, R. R., & Espinosa Zaragoza, S. (2017). Extractos por destilación de Origanum vulgare, Tradescantia spathacea y Zingiber officinale para el manejo de Moniliophthora roreri de Theobroma cacao. Revista Mexicana de Ciencias Agrícolas, 7(5), 1065–1076. https://doi.org/10.29312/remexca.v7i5.232
Torres-De la Cruz, M., Quevedo-Damián, I., Ortiz-García, C. F., Lagunes-Espinoza, L. C., Nieto-Ángel, D., & Pérez-De la Cruz, M. (2019). Control químico de Moniliophthora roreri en México. Biotecnia, 21, 55–61. https://doi.org/10.18633/biotecnia.v21i2.906
Wang, T., Li, Q., Zhang, H., & Chen, J. (2024). Flavonoids from Citrus reticulata: Inhibitory activity against pathogenic fungi and biocontrol potential. Physiological and Molecular Plant Pathology, 131, 102250. https://doi.org/10.1016/j.pmpp.2024.102250
Xu, D., Deng, Y., Han, T., Jiang, L., Xi, P., Wang, Q., Jiang, Z., & Gao, L. (2018). In vitro and in vivo effectiveness of phenolic compounds for the control of postharvest gray mold of table grapes. Postharvest Biology and Technology, 139, 106–114. https://doi.org/10.1016/j.postharvbio.2017.08.019
Xu, H., Wang, G., Zhang, J., Zhang, M., Fu, M., Xiang, K., Zhang, M., & Chen, X. (2022). Identification of phenolic compounds and active antifungal ingredients of walnut in response to anthracnose (Colletotrichum gloeosporioides). Postharvest Biology and Technology, 192, 112019. https://doi.org/10.1016/j.postharvbio.2022.112019
Yang, W., Zhang, L., Yang, Y., Xiang, H., & Yang, P. (2024). Plant secondary metabolites-mediated plant defense against bacteria and fungi pathogens. Plant Physiology and Biochemistry, 217, 109224. https://doi.org/10.1016/j.plaphy.2024.109224